Rivista di formazione e aggiornamento di pediatri e medici operanti sul territorio e in ospedale. Fondata nel 1982, in collaborazione con l'Associazione Culturale Pediatri.
Maggio 2010 - Volume XIII - numero 5
M&B Pagine Elettroniche
Contributi Originali - Casi contributivi
Epilessia
con mioclonie palpebrali e assenze
1Scuola
di Specializzazione in Pediatria, Università di Ferrara
2Clinica
Pediatrica Universitaria, Arcispedale S. Anna, Ferrara
Indirizzo
per corrispondenza: luciamarangio@yahoo.it
Eyelid
myclonia with absences, EMA
Keywords
Idiopathic
generalized epilepsy, Video-EEG, Eyelid myoclonia with absences,
Tic, Photosensitivity
Summary
Eyelid
myoclonia with absences (or Jeavons syndrome) is an idiopathic
reflex generalized epilepsy, which has unique clinical and EEG
features. It is characterised by the triad of: 1. eyelid
myoclonia with and without absences; 2. eye closure-induced
seizures, EEG paroxysms or both; 3. photosensitivity. The
syndrome is not very frequent and is not well recognized in the
paediatric population. We report the case of two children in whom
eyelid myoclonia with absences was misdiagnosed as facial tics. |
|
Parole
chiave
Epilessia
Idiopatica Generalizzata, Epilessia con mioclonie palpebrali e
assenze, Tic, Fotosensibilità, Video-EEG.
Riassunto
LEpilessia
con mioclonie palpebrali e assenze (EMA, o Sindrome di Jeavons) è
una forma non comune di epilessia riflessa idiopatica generalizzata,
con manifestazioni cliniche ed EEG molto ben definite. È
caratterizzata dalla triade sintomatologica: 1. Mioclonie palpebrali
con o senza assenze; 2. Crisi cliniche, scarica EEG (o entrambe)
indotte dalla chiusura degli occhi; 3. Fotosensibilità.
Riportiamo 2 casi di EMA in cui si è verificato ritardo
diagnostico, dovuto ad errata diagnosi di sindrome ticcosa.
C., 5
anni. Nata da taglio cesareo urgente per sofferenza fetale. Nel primo
anno di vita, sviluppo psico-motorio riferito nella norma,
deambulazione a 13 mesi. Dalletà di 2 anni la bambina
veniva seguita da un servizio di neuropsichiatria infantile per
ritardo del linguaggio, difficoltà di comprensione di ordini
più complessi e frasi articolate. Alletà di 4
anni, a tale corteo sintomatologico, si aggiungevano episodi di
ammiccamento oculare pluriquotidiano, accentuati dalle situazioni di
stress e dalla luce molto intensa, di brevissima durata, talvolta
associati a revulsione dei bulbi oculari, retropulsione del capo, e
attimi di lieve perturbazione della coscienza. Questi fenomeni per
ben due anni sono stati interpretati come tic, continuando il
percorso terapeutico con i neuropsichiatri.
La
persistenza dei sintomi ha portato ad un approfondimento diagnostico,
con valutazione neurologica pediatrica e studio neurofisiologico.
I., 3
anni. Nato da parto eutocico da gravidanza normodecorsa.
Deambulazione a 20 mesi. Seguito per ritardo del linguaggio alletà
di 2 anni. Durante un ricovero in Clinica Pediatrica per episodio
febbrile di natura virale, vengono osservati numerosi episodi
caratterizzati da chiusura prolungata degli occhi, seguita da lieve
perturbazione della coscienza e revulsione dei bulbi oculari, della
durata di circa 2 secondi. Dallanamnesi emerge che gli episodi
di chiusura degli occhi, interpretati dai genitori come tic, sono
comparsi circa 2 mesi prima, e che si verificano soprattutto quando
il bimbo è contrariato e arrabbiato. Il bimbo viene dunque
inviato allosservazione del Neurologo Pediatra e studio
elettroencefalografico (EEG).
Studio
EEG
È
stato effettuato uno studio EEG standard con registrazione Video-EEG
in veglia in presenza di normale luce ambientale: in entrambi i casi
entro 1 secondo dalla chiusura degli occhi sono comparse scariche
generalizzate di punta-onde, di durata inferiore ai 3 secondi, a cui
si associa clinicamente il fenomeno motorio della mioclonia
palpebrale. In entrambi i soggetti la chiusura degli occhi in
presenza di oscurità ambientale non ha provocato alcuna
scarica EEG, né alcun fenomeno clinico. La stimolazione
luminosa intermittente ha determinato risposta foto-parossistica in
entrambi i casi.
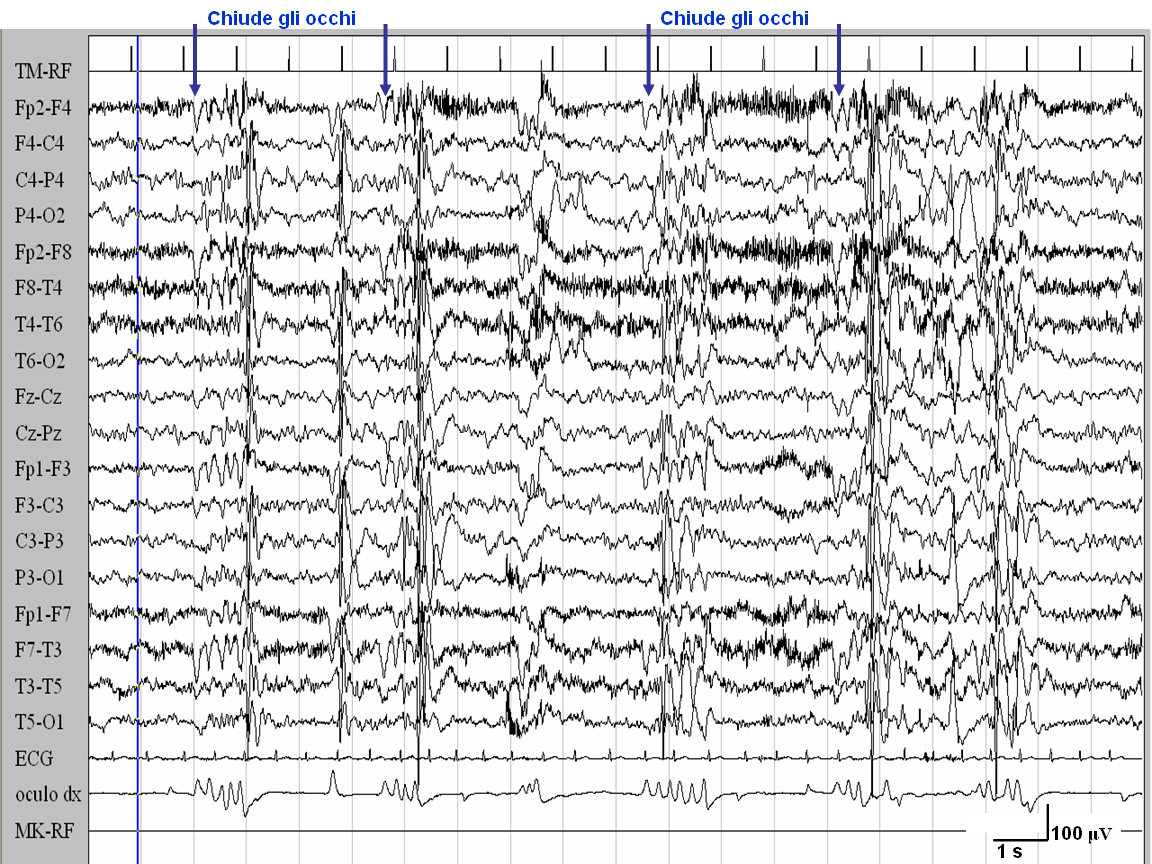
Caso
1. numerose scariche di punte-onde ed onde lente, che compaiono dopo
la chiusura degli occhi
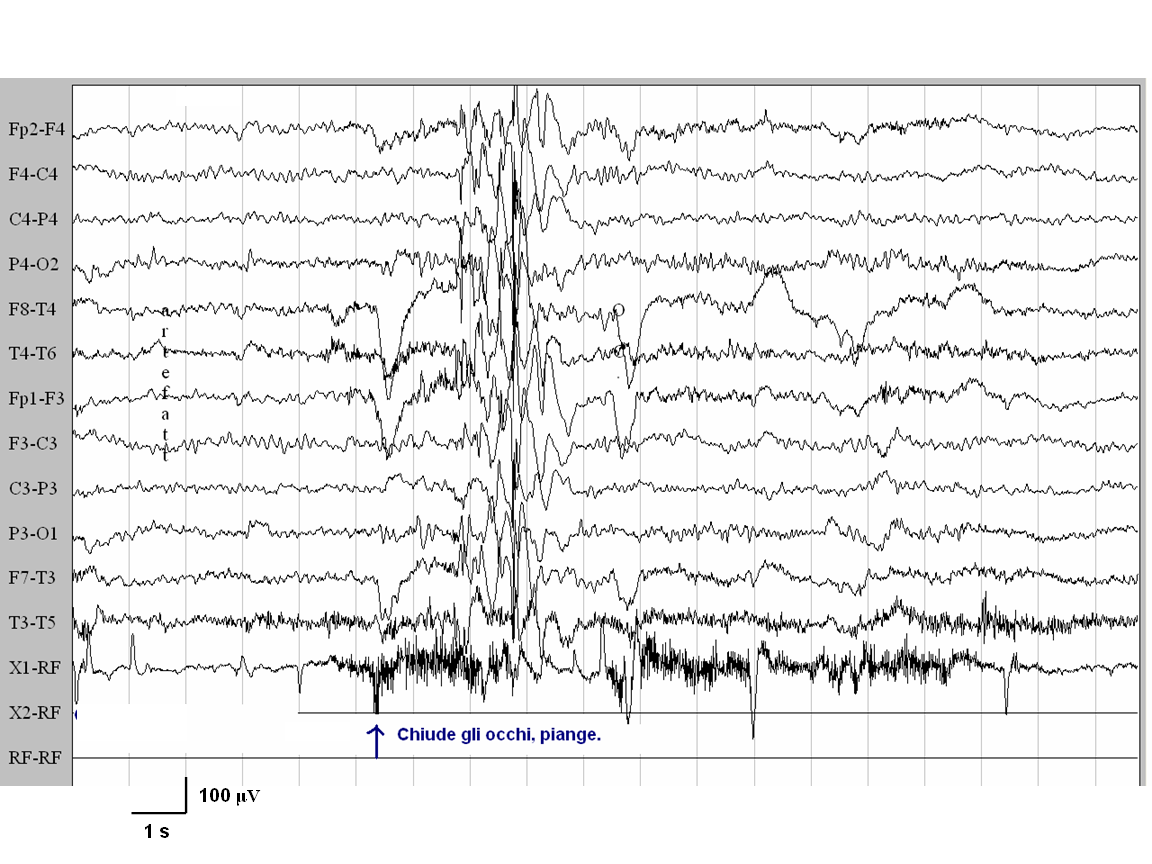
Caso
2. dopo la chiusura degli occhi compare una scarica generalizzata di
punte-onde di elevato voltaggio, a 3 cicli al secondo
Gli
eventi clinici ed elettroencefalografici descritti nei nostri due
pazienti sono compatibili con la diagnosi di Epilessia con mioclonie
palpebrali ed assenze.
Descritta
inizialmente da Jeavons nel 1977 come una forma di epilessia
fotosensibile, non è stata inserita ufficialmente nella
Classificazione Internazionale delle Epilessie attualmente in uso1,
nonostante le sue caratteristiche siano state ben definite. Le
mioclonie palpebrali, con o senza assenze, sono state invece
riconosciute come tipo di crisi a sé stante nella revisione
della Classificazione del 2001. Sono crisi che occorrono in molte
condizioni epilettiche idiopatiche, sintomatiche o probabilmente
sintomatiche2.
La
frequenza di tale sindrome tra i pazienti epilettici è stimata
tra l1.25% e il 2.7%, con prevalenza nel sesso femminile (come
tutte le epilessie fotosensibili)3. La prevalenza è intorno al
3% negli adulti epilettici, e del 13% negli adulti con epilessie
idiopatiche generalizzate. Lesordio è tipicamente
nellinfanzia, tra i 2 e 14 anni, con un picco intorno ai 6-8
anni1.
La
sindrome ha evidenti caratteri di familiarità, i cui aspetti
genetici sono però ancora poco noti3.
Lelemento
caratterizzante della Sindrome di Jeavons sono le mioclonie
palpebrali, che si presentano marcate, rapide, a tipo di flutter
o fremito palpebrale, associate a versione verso lalto dei
globi oculari e retropulsione del capo. Le crisi, brevi (3-6sec) e
pluriquotidiane, compaiono con una latenza di 0.5-2 sec dalla
chiusura degli occhi (sia essa volontaria, involontaria o riflessa)
in un ambiente luminoso.
Lespressività
clinica delle mioclonie palpebrali può essere varia: nel caso
1 la bambina presentava un evidente ammiccamento oculare, cioè
una apertura e chiusura veloce delle palpebre che non poteva passare
inosservata, anche se male-interpretata; il bambino del secondo caso
invece mostrava episodi di chiusura prolungata degli occhi, e la
mioclonia palpebrale era di modestissima entità, quasi
impercettibile.
Talora a
questo tipico fenomeno motorio si associano assenze, con
perturbazione della coscienza che può anche essere molto
lieve, come nei due casi presentati.
Controverso
è il fenomeno dellautoinduzione delle crisi 1,4.
Un rilevante fattore di confondimento è la convinzione diffusa
in ambito medico che la mioclonia palpebrale sia un tentativo
consapevole di auto-indurre le crisi: il corrispondente clinico della
crisi elettrica è invece proprio la mioclonia palpebrale, che
è scatenata dalla chiusura degli occhi e può essere
seguita o no da una assenza. Secondo lesperienza di
Panayotopoulos, le crisi auto-indotte sono rare; comunque, i pazienti
potrebbero essere non deliberatamente auto-induttori, ma soffrire di
una auto-induzione compulsiva, similmente alla sintomatologia
descritta nella sindrome di La Tourettes1. In entrambi i
casi descritti i fenomeni aumentano se i bambini sono contrariati o
arrabbiati con i loro genitori: questo ci fa supporre che siamo di
fronte a due casi si auto-induzione delle crisi. In particolare il
bambino del caso 2 strizza volontariamente gli occhi (e di
conseguenza provoca le crisi epilettiche) quando non vuole eseguire i
compiti che gli vengono richiesti.
Crisi
Tonico-Cloniche Generalizzate, indotte dallo stimolo visivo oppure
spontanee, sono presenti in oltre il 50% dei casi, soprattutto in
soggetti di età adolescenziale. Queste manifestazioni possono
rappresentare il motivo della prima consultazione e le mioclonie
palpebrali essere riconosciute solo retrospettivamente. Raramente
compaiono scosse miocloniche a carico degli arti inferiori. Nel 20%
dei casi è possibile il verificarsi di uno Stato di Male,
anchesso caratterizzato da episodi ripetitivi e continui di
mioclonia palpebrale con lievi assenze.
LEEG
e la registrazione VIDEO-EEG sono procedure diagnostiche
fondamentali5: le manifestazioni EEG critiche consistono
principalmente di scariche generalizzate di 3-5 complessi di punte o
polipunte-onde, a 3-6 Hz. Le scariche sono brevi (1-6 sec), e
compaiono tipicamente entro 0.5-2 sec dalla chiusura degli occhi in
presenza di luce; allevento elettrico corrisponde spesso
levento clinico della mioclonia palpebrale. Le scariche EEG
possono essere attivate anche dalliperventilazione. Durante il
sonno, le scariche sono più brevi e prive di alcun correlato
clinico discernibile. La chiusura degli occhi in oscurità
totale non provoca alcuna anomalia EEG, né crisi clinica.
Tutti i
pazienti, come i due casi descritti, sono fotosensibili, cioè
presentano una anomala risposta agli stimoli luminosi, evidenziata
durante la registrazione EEG come una reazione parossistica alla
stimolazione luminosa intermittente (SLI). Questo fenomeno elettrico,
elicitato dalla SLI o da stimoli visivi della vita quotidiana, è
denominato risposta foto-parossistica (Photo
Paroxysmal Response, PPR) 6.
La EMA si
distingue dalle altre forme di epilessie fotosensibili, in quanto
questi pazienti sono sensibili sia alla SLI che alla luce brillante
continua non intermittente (le altre epilessie fotosensibili
rispondono solo alla SLI), e per il fatto che la chiusura degli occhi
è comunque un fattore scatenante molto più potente
della foto stimolazione7.
Il
fenomeno della fotosensibilità si può osservare in
molti tipi di epilessie o al di fuori di casi di epilessia
clinicamente evidenti. La prevalenza in soggetti non epilettici varia
dallo 0,5 all8.9% della popolazione, e raramente questo
fenomeno evolve in epilessia. In soggetti epilettici la risposta alla
SLI è stata trovata in circa il 10-20% dei bambini e 5-10%
degli adulti 8; in tale popolazione il PPR può essere un
riscontro occasionale, ma più frequentemente è
strettamente correlato al tipo di epilessia in questione 6.
La
fotosensibilità è più frequente nella tarda
infanzia e prima adolescenza. Alcuni autori hanno riportato un picco
dincidenza tra 11 e 15 anni e hanno notato che questa si
riduce drammaticamente dopo i 20 anni. Le femmine sono più
coinvolte ad ogni età: questo per differenze ormonali (che
potrebbero anche essere la causa dellesordio età-correlato),
o in alternativa per leffetto di fattori patogenetici genetici
o epigenetici, correlati ai 2 cromosomi X (ginecotropismo) o dovuto
agli effetti protettivi diretti o indiretti del cromosoma Y9.
In
passato è stata segnalata la possibilità che la
frequenza di PPR potesse variare tra le popolazioni che vivono in
regioni del mondo con diverse quantità di luce, in realtà
oggi si sa che questa differenza è legata a fattori genetici.
Proprio la presenza nella EMA di costante e marcata fotosensibilità
la rende un modello di studio ideale della genetica di questo
fenomeno.
La
fotosensibilità non costituisce una sindrome epilettica di per
sé, può essere propria di tutte le principali categorie
di disordini epilettici (Tabella 1)
caratteristica dellEMA6.
generalized
epilepsies
1.
idiopathic generalized epilepsies (ige), in order of age
a.benign
myoclonic epilepsy of infancy (included late and reflex variants)
b.childhood
absence epilepsy
c.juvenile
absence epilepsy
d.juvenile
myoclonic epilepsy
e.gtcs
on awakening
f.ige
with practice-induced seizures, including primary reading epilepsy
g.visual
sensitive ige, including eyelid myoclonus with absences
2.
cryptogenic generalized epilepsies
a.epilepsy
with myoclonic-astatic seizures (doose syndrome)
3.
symptomatic generalized epilepsies
a.progressive
myoclonus epilepsies
neuronal
ceroid lipofuscinosis (late infantile, adult forms)
laforas
disease
unverrichtlundborg
disease
myoclonus
epilepsy with ragged-red fibers (merrf)
b.gaucher
(type iii, neuronopathic form)
c.other
forms
localization-related
epilepsies
1.
idiopathic partial epilepsies
a.idiopathic
visual sensitive occipital lobe epilepsy
2.
symptomatic and cryptogenic partial epilepsies
undetermined
epilepsies
1.
severe myoclonic epilepsy of infancy (dravet syndrome)
situation-related
and occasional seizures
1.
strong provocative visual stimuli in patients with latent vs
2.
alcohol withdrawal, drugs, vitamins, toxic drugs |
Tabella
1. Classificazione sindromica delle epilessie fotosensibili
(adattata da Kasteleijn-Nolst Treint DG et al, 2001 10).
La
corteccia cerebrale gioca un ruolo fondamentale nella genesi delle
manifestazioni elettrocliniche delle epilessie fotosensibili. La
corteccia frontorolandica (CFR) ed occipitale (CO) sembrano essere le
più coinvolte nella generazione di risposte anormali. La SLI
sincronizza i neuroni della CO (CO), mediante le due
vie principali del sistema visivo: magnocellulare e parvocellulare.
(Figura 1).
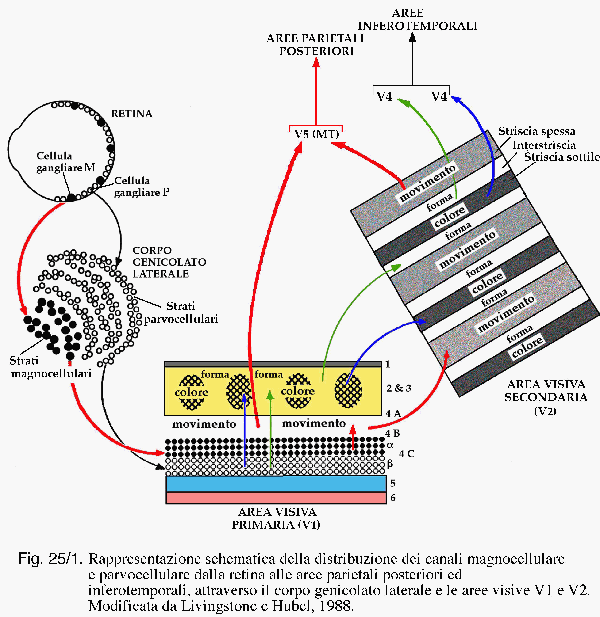
Figura
1. Rappresentazione schematica della distrbuzione dei canali
magnocellulare e parvocellulare dalla retina alle aree parietali
posteriori ed inferotemporali, attravewrso il corpo genicolarto
laterale ele aree visive V1 e V2.
Lattivazione
della CO dipende dallintensità della luce, dal volume
di corteccia attivato e dal livello di eccitabilità. La
diffusione della risposta visiva in particolare alla CFR è
possibile o attraverso vie trans-corticali o sottocorticali
(reticolo-talamiche), ed induce scariche neuronali generalizzate o
prevalentemente parossistiche frontorolandiche. Le interazioni
talamo-corticali reciproche sono probabilmente essenziali per
generare punte e onde ritmiche (e assenze) che seguono liniziale
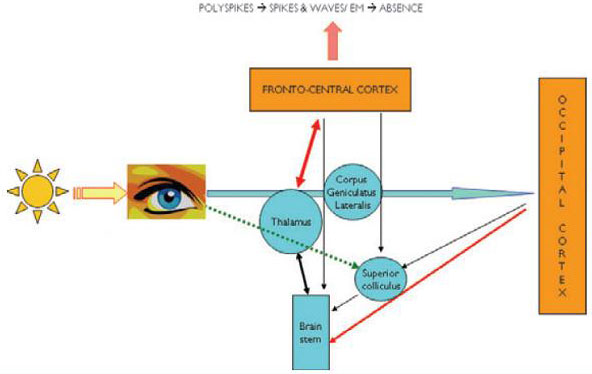
polipunta (e mioclonia)11,12 (Figura
2).
Su questo
substrato neurofisiologico, nel soggetto in cui
lipersincronizzazione e liperattivazione
neuronale dipende probabilmente dallalterazione
funzionale geneticamente determinata delle vie parvo- e
magno-cellulari e del generatore del ritmo α, 7, lo stimolo
visivo (chiusura degli occhi in ambiente illuminato) produce le
caratteristiche cliniche (mioclonia palpebrale, GTCS) ed
elettroencefalografiche (risposta fotoparossisitica) della EMA. Di
conseguenza, lattenuazione della luce inibisce la risposta
alla chiusura degli occhi nellEMA, così come la
stimolazione monoculare o le lenti ottiche riducono la risposta alla
foto stimolazione nei pazienti fotosensibili, ed alcuni farmaci
antiepilettici e la riduzione età correlata delleccitabilità
riducono la diffusione delle scariche, limitando lattività
parossistica alla corteccia posteriore11.
Il
fenomeno della fotosensibilità è un problema della
quotidianità, conosciuto sin dallantichità: per
evitare lacquisto di schiavi epilettici si faceva girare una
ruota interposta tra loro ed il sole, provocando così uno
stimolo luminoso intermittente in grado di scatenare la crisi
epilettica. Per restare in ambito lavorativo,
lutilizzo di display o pc con programmi standard utilizzabili
per studio od in ufficio (es. Word) è una causa non frequente
di scatenamento di crisi, a meno che, ovviamente, il computer non sia
usato ad altri scopi.
Se il
soggetto è collocato a meno di 2 metri di distanza da uno
schermo con date caratteristiche fisiche (frequenza 50/60 Hz) e se
vengono proiettate immagini con determinate caratteristiche fisiche è
molto probabile che levento critico sia scatenato. È
quello che è accaduto nel cosiddetto incidente dei
Pokemon in Giappone, in cui numerosi pazienti ebbero una crisi
epilettica durante la visione di un determinato episodio del famoso
cartone animato, caratterizzato da una specifica combinazione di
stimoli visivi complessi (pattern visivo a strisce, con alternanza di
colore rosso e blu). È chiara lentità del
problema nella popolazione pediatrica attuale che fa largo uso di
televisione, computer e videogiochi nella vita quotidiana. A tal
proposito, negli ultimo anni, misure preventive specifiche riguardo
le caratteristiche fisiche degli schermi (frequenza 100 Hz) e delle
immagini contenute nei videogiochi in commercio hanno portato ad una
riduzione del problema.
Sono
comunque molte le situazioni che possono provocare crisi in cui un
soggetto fotosensibile, soprattutto in presenza di fattori favorenti
quali la deprivazione da sonno, lo stress, luso di alcool6.
Di fronte
al sospetto di un evento epilettico, che nei nostri casi era
sostenuto soprattutto dalle caratteristiche associate alla mioclonia
palpebrale (le assenze e la revulsione dei globi oculari), un
approfondimento neurofisiologico è dunque dobbligo e
nella totalità dei casi lEEG è diagnostico e
dirimente.
La
presenza di anamnesi positiva per mioclonie palpebrali associata alle
caratteristiche EEG sopra descritte è molto suggestiva di
diagnosi di sindrome di Jeavons, che tuttavia è spesso
misconosciuta in quanto i fenomeni più lievi possono essere
confusi con tic facciali, talvolta per molti anni13,14.
I bambini
dei casi 1 e 2 sono giunti allattenzione del neurologo
pediatra rispettivamente con posta e sospetta pregressa diagnosi di
sindrome ticcosa. Di fronte ad un paziente che presenta mioclonia
palpebrale si pone infatti il problema della diagnosi differenziale
tra i vari disturbi del movimento che possono comparire
nellinfanzia, tra cui appunto i tic motori (Tabella
2 e Tabella 3).
Pur
essendo lammiccamento oculare una delle più frequenti
manifestazioni ticcose, queste tendono a variare nelle loro
caratteristiche con il tempo, e solitamente si associano ad altre
manifestazioni ticcose, motorie e non 15,16.
Poniamo
quindi il sospetto di Sindrome di Jeavons quando la mioclonia
palpebrale si presenta con le seguenti caratteristiche:
Monomorfismo
della manifestazione, altamente stereotipata;
Associata
a revulsione bulbi oculari e/o retropulsione capo;
Compresenza
di riduzione del contatto, anche lieve;
- tic motori- semplici (ammiccamento delle palpebre)- complessi (grattarsi, saltellare)- elaborati (camminare a cerchio)- distonici (movimenti prolungati)tic fonici- semplici (tossire, sbuffare, raschiarsi la gola)- complessi (espressioni non intelligibili)- eloquio irregolare (esplosivo, coprolalico, ecolalico)tic sensoriali- sensazioni somatiche ricorrenti e sgradevoli
- tic motorioMovimento spasmodico, involontario, ripetitivo, stereotipato, non ritmico, spesso esacerbato dallo stress. Può coinvolgere qualsiasi gruppo muscolare. Vissuto come irrefrenabile, può essere controllato mediante la volontà solo per breve tempo, si attenua molto durante il sonno e può preceduto da unaura caratterizzata dalla sensazione di bisogno urgente che il TIC si compia, con successivo senso di sollievo.mioclonoContrazione breve e involontaria di un muscolo o di gruppi muscolari (simultanea contrazione di agonista+antagonista) che può non produrre spostamento o dare movimenti sia regolari o talvolta irregolari (mioclono massivo, segmentale o parcellare). Durata del mioclono< 80 mstremoreMovimenti oscillanti e persistenti, con frequenza fissa. Possono essere statici, posturali, intenzionali. Contrazione alternata di muscoli agonisti e antagonisti. Possono essere più o meno rapididistoniaContrazione di muscoli agonisti e antagonisti che causa posture anomale, talvolta dolorose e prolungatecoreaMovimenti bruschi, di breve durata, irregolari e continuamente mutevoli (muscolatura distale, tronco, volto)atetosiMovimenti involontari di torsione, costanti ma lenti, è un disturbo del centro nervoso centrale, caratterizzato da movimenti continui, senza coordinazione degli artimanierismiParticolari arricchimenti motori che alcune persone sviluppano mentre eseguono certi movimenti o gesti. Questi manierismi sono fenomeni volontari normali; tuttavia in alcuni casi possono sembrare anormali in particolare se il manierismo fa assumere posture inusuali.spasmiContrazione improvvisa e involontaria di un muscolo (o un gruppo di muscoli) a volte accompagnato da un repentino "scoppio" di dolore ma di solito è innocuo e cessa dopo pochi minuti
La
sindrome di Jeavons va anche distinta da altre condizioni
epilettiche, con cui ha in comune alcuni elementi11
(Tabella 4), ma da cui si discosta
per le peculiarità elettro-cliniche; in particolare va
differenziata dallEpilessia con assenze dellInfanzia
(Piccolo Male), una delle forme più note e frequenti di
epilessia infantile. Lelemento caratterizzante di questo
quadro sono le assenze, che sono pluriquotidiane, di durata tra 4 e
20 sec, e comportano unalterazione della coscienza improvvisa
e severa; possono associarsi lievi mioclonie palpebrali nei primi 3
secondi dellassenza, ma esse sono un elemento marginale e non
costante del quadro, e comunque mancano del nesso temporale e causale
con la chiusura degli occhi, proprio della EMA. Anche il tracciato
EEG ha caratteristiche ben definite: scariche generalizzate di
punte-onde, ritmiche, con frequenza di 3Hz18.
- Condizioni con sensibilità alla chiusura degli occhi
- Eyelid myoclonia with absences
- Juvenile absence epilepsy
- Juvenile myoclonic epilepsy
- Idiopathic generalized epilepsy with tonicclonic seizures
- Idiopathic occipital lobe epilepsy
Condizioni con mioclonia palpebrale (con o senza assenze)- Eyelid myoclonia with absences
- Childhood absence epilepsy
- Juvenile absence epilepsy
- Juvenile myoclonic epilepsy
- Sunflower syndrome(s)
- Self-induced seizures
- Idiopathic generalized epilepsy with phantom absences
- Myoclonic status in nonprogressive encephalopathies
Condizioni con fotosensibilità- Eyelid myoclonia with absences
- Visual reflex seizures
- Sunflower syndrome(s)
- Benign myoclonic epilepsy in infancy
- Childhood absence epilepsy
- Juvenile myoclonic epilepsy
- Idiopathic generalized epilepsy with tonicclonic seizures
- Juvenile absence epilepsy
- Idiopathic photosensitive occipital lobe epilepsy
- Severe myoclonic epilepsy of infancy (Dravet syndrome)
- Progressive myoclonic epilepsies
- Alcohol or benzodiazepines withdrawal
Tabella
4. Condizioni epilettiche con caratteristiche comuni alla
Epilessia con mioclonie palpebrali ed assenze (adattata da Striano et
al, 200911)
LEpilessia
con mioclonie palpebrali e assenze è una patologia a lungo
termine, con prognosi migliore nel sesso maschile. Poiché di
recente identificazione, i follow up dei pazienti sono ancora scarsi.
Per
migliorare la qualità di vita di questi pazienti, è
importante adottare alcune strategie volte a limitare lo scatenamento
delle crisi, come soggiornare in presenza di ridotta luminosità
ambientale o indossare speciali lenti ottiche. Utili sono gli
accorgimenti consigliati in tutte le epilessie fotosensibili (Tabella
5)6, ma è da sottolineare il fatto che oggi,
nella realtà moderna in cui viviamo, è sempre più
difficile essere sottoposti a determinati stimoli visivi.
Proprio
per questo motivo nella maggior parte dei pazienti è
necessario lutilizzo di farmaci antiepilettici. La terapia
farmacologia della EMA si basa tuttoggi su evidenze
aneddotiche, in quanto non esistono trial terapeutici controllati che
diano indicazioni precise. Lapproccio tradizionale prevede
farmaci impiegati nella terapia delle altre epilessie idiopatiche
generalizzate con assenza e mioclonie: il farmaco di prima scelta è
il Valproato (VPA) in monoterapia, che presenta percentuali di
efficacia variabili tra il 73 e l86%12. Al VPA si
possono affiancare altri farmaci: lassociazione con
lEtosuccimide è considerata la più efficace; il
Clonazepam può essere utilizzato in caso di mioclono agli arti
inferiori, il fenobarbital per il controllo delle Scosse
Tonico-Cloniche Generalizzate (GCTS)19. Le crisi di
assenza sono sensibili alla terapia, diminuendo di frequenza, e anche
il fenomeno della fotosensibilità, che dì per sé
si riduce con letà fino a scomparire in adolescenza,
risponde bene ai farmaci.
Le
mioclonie palpebrali sono invece frequentemente resistenti al
trattamento e possono persistere anche in età adulta, con
frequenza pluriquotidiana. Nel 2008 è stato pubblicato uno
studio sullutilizzo del Levetiracetam nella sindrome di
Jeavons, un farmaco antiepilettico di nuova generazione, con
meccanismo dazione, farmacocinetica, tollerabilità ed
efficacia dimostrata in popolazione sia adulta che pediatrica, con
ben note proprietà antimiocloniche 20. Gli autori riportano
una buona efficacia nel controllo della mioclonia palpebrale e delle
GCTS alla dose di 50.60mg/kg/day, somministrati in mono- o
poli-terapia, con una riduzione delle crisi nell80% dei
pazienti studiati.
Suggeriscono
inoltre la possibilità, in casi selezionati di EMA, di
utilizzare il levetiracetam come farmaco di prima scelta, e non come
terapia aggiuntiva o sostitutiva nel momento del fallimento della
terapia con un farmaco tradizionale. Nei casi in cui si sospetti
lautoinduzione delle crisi si consiglia supporto
neuropsichiatrico.
-Avoid
potentially provocative stimuli: discotheque, flickering sunlight,
flashing TV programs and VGs, striped patterns
-Use
of small TV, 12-in set
-Use
100-Hz screen
-Use
of a lamp beside the TV
-Use
of temporal optical filter
-Use
of remote control
-Respect
critical distance of 2 m from the screen
-Monocular
occlusion in case of exposition to trigger stimuli
-Avoid
stress, extreme fatigue, sleep deprivation
-Avoid
prolonged videogames playing (>1 h per session)
-Avoid
playing videogames if suffering from lack of sleep
-Avoid
playing videogames alone
-Use
of glasses: dark, polarized, colored lenses |
È
auspicabile la precoce identificazione e trattamento della sindrome
di Jeavons, dal momento che un ritardo diagnostico può
verosimilmente interferire con lo sviluppo neuro-psicologico del
piccolo paziente: nel caso 1 non veniva comunque segnalato dai
neuropsichiatri che seguivano la piccola una progressiva regressione
delle funzioni in via di sviluppo, dopo la diagnosi è stata
intrapresa terapia con valproato ed etosuccimide, con successo nel
controllo delle assenze, ma non delle mioclonie palpebrali e della
fotosensibilità. Non è stato possibile seguirne il
follow up in quanto la paziente non è più seguita
presso il nostro centro; possiamo affermare che sarebbe stata una
candidata ideale allimpiego del Levetiracetam. Il bambino del
caso 2 invece è risultato responsivo alla terapia con
valproato e clonazepam, con riduzione pressoché totale delle
assenze, delle mioclonie e della fotosensibilità, e
conseguente netto miglioramento del quadro neuropsicologico.
Per
concludere, è importante ricordare che la sindrome di Jeavons
esiste ed è sottostimata perché spesso le sue
manifestazioni più sfumate non sono colte oppure sono confuse
con una sindrome ticcosa; che in presenza di un bambino con tic, non
bisogna banalizzare il quadro, ma saper cogliere quelle particolarità
che possano far sorgere il sospetto che possa trattarsi di
qualcosaltro; ricordare che anche solo il sospetto (non è
necessaria la certezza) di trovarsi di fronte ad una forma epilettica
giustifica linvio del paziente ad una valutazione
specialistica neurologica con studio neurofisiologico, soprattutto in
questo caso in cui la registrazione EEG è sempre diagnostica,
e permette di identificare una epilessia che, intrapresa la terapia
adeguata, anche alla luce dellavvento dei nuovi farmaci
antiepilettici, è suscettibile di miglioramento clinico, con
indubbio guadagno del paziente dal punto di vista dello sviluppo
neuropsicologico.
Bibliografia
- Panayiotopoulos C.P. Syndromes of Idiopathic Generalized Epilepsies Not Recognized by the International League Against Epilepsy. Epilepsia 2005; 46:57-66.
- Engel J. A proposed Diagnostic Scheme for people with epileptic seizure and with epilepsy: report of the ILAE Task Force on classification and terminology. Epilepsia 2001; 42:796803.
- Capovilla G, Rubboli G, Striano S. et al. Proposta di studio genetico e clinico-neurofisiologico della sindrome mioclonie palpebrali con assenze. www.lice.it/LICE_ita/commissioni/pdf/protocollo_ema.pdf
- Beng-Yeong Ng. Psychiatric aspects of self-induced epileptic Seizures. Australian and New Zealand Journal of Psychiatry, 2002; 36:53443.
- Joshi CN, Patrick J. Eyelid myoclonia with absences: Routine EEG is sufficient to make a diagnosis. Seizure 2007;16:254-60.
- Verrotti A, Tocco AM, Salladini C, Latini G, Chiarelli F. Human photosensitivity: from pathophysiology to treatment. European Journal of Neurology 2005;12: 8284.
- Panayiotopoulos CP. Reflex seizure and reflex epilepsies. In: Panayiotopoulos CP. A clinical guide to epileptic syndromes and their treatment. 2th edition, Società editrice Springer, 2007: 437-68.
- Fisher RS, Harding G, Erba G, Barkley GL, Wilkins A. Photic- and Pattern-induced Seizures: A Review for the EpilepsyFoundation of America Working Group. Epilepsia 2005;46(9):142641.
- Ulrich Stephani, Genetics of Photosensitivity (Photoparoxysmal Response): A ReviewEpilepsia 2004; 45(Suppl. 1):1923.
- Kasteleijn-Nolst Treint DG, Guerrini R, Binnie CD, Genton P. Visual sensitivity and epilepsy: a proposed terminology and classification for clinical and EEG phenomenology. Epilepsia 2001;42:692701
- Striano S, Capovilla G, Sofia V et al. Eyelid mioclonia with absences (Jeavon syndrome): A well-defined idiopatica generalized epilepsy syndrome or a spectrum of photosensitive conditions?. Epilepsia 2009;50 (5):15-9.
- Covanis A. Photosensitivity in idiopathic generalized epilepsies. Epilepsia 2005;46(6):67-72.
- Incorpora G, Sofia V, Pavone P, Biondi R, Barone B, Parano E. Clinical heterogeneity in eyelid myoclonia, with absences and epilepsy. Eur J Pediatr 2002;161:1757.
- Striano S, Striano P, Nocerino C et al. Eyelid myoclonia with absences: an overlooked epileptic syndrome? Neurophysiologie Clinique 2002;32:287-96.
- Dooley J. Tic Disorders in Childhood. Semin Pediatr Neurol 2006;13:231-42.
- Delgado MR, Leland Albright A. Movement Disorders in children: definitions, classifications, and grading systems. J Child Neurol 2003;18:S1-S8.
- Dressler D. et al., Diagnosis and management of acute movement disorders. J Neurol 2005; 252:1299-1306.
- Panayiotopoulos CP. Idiopathic generalised epilepsies. In: Panayiotopoulos CP. A clinical guide to epileptic syndromes and their treatment. 2th edition, Società editrice Springer, 2007: 325-330.
- Panayiotopoulos CP. Eyelid myoclonia with and without absences. www.ilae-epilepsy.org/ctf/eyelid_myoclonia_w_wo_abs.html
- Striano P, Sofia V, Capovilla G et al. A pilot trial of levetiracetam in eyelid myoclonia with absences (Jeavons syndrome). Epilepsia 2008;49(3):42530.
Vuoi citare questo contributo?
