Rivista di formazione e aggiornamento di pediatri e medici operanti sul territorio e in ospedale. Fondata nel 1982, in collaborazione con l'Associazione Culturale Pediatri.
Marzo 2007 - Volume X - numero 3
M&B Pagine Elettroniche
Appunti di Terapia
Linee
guida per l'uso del vaccino pentavalente contro i rotavirus
(RotaTec)
Membro
della Commissione Nazionale Vaccini
Indirizzo
per corrispondenza: bartolozzi@unifi.it
Il 3
febbraio 2006, un vaccino pentavalente, basato su virus di origine
bovina, contro i rotavirus (RotaTeq, Merck & Co) è stato
approvato dalla Food and Drug statunitense, per l'uso nei
lattanti degli Stati Uniti.
L'Accademia
Americana di Pediatria raccomanda l'immunizzazione routinaria dei
lattanti, con 3 dosi di vaccino pentavalente, somministrato per bocca
a 2, 4 e 6 mesi di età. La prima dose va somministrata in
bambini in età fra le 6 e le 12 settimane di età; la
vaccinazione non deve essere iniziata dopo la 12° settimana di
età. Le due dosi successive vanno somministrate da 4 a 10
settimane d'intervallo, ma tutte le dosi vanno usate entro le 32
settimane di età, corrispondenti all'ottavo mese di vita.
Il
vaccino pentavalente contro i rotavirus può essere
co-somministrato con tutti gli altri vaccini, presenti in calendario.
Esso è controindicato per i lattanti che abbiamo gravi
reazioni allergiche verso qualsiasi componente del vaccino o verso
dosi precedentemente somministrate.
Nel
fascicolo di gennaio 2007 del Pediatrics sono comparse le Linee Guida
per l'uso di questo vaccino (AAP. Committee on Infectious Diseases.
Prevention of rotavirus disease: guidelines for use of rotavirus
vaccine. Pediatrics 2007, 119:171-81). Questo vaccino non è in
commercio in Italia.
Per ora
in Italia è in commercio un altro vaccino contro i rotavirus,
quello della GlaxoSmithKline, dal nome Rotarix,, costituito da
rotavirus umano, ceppo RIX4414 (vivo attenuato), in quantità
non meno di 106 CCID50 per dose da 1 mL., prodotto su cellule lineari
Vero: questo vaccino viene somministrato in due dosi, di cui la prima
a partire dalla 6° settimana di vita e la seconda dopo 4
settimane: comunque il ciclo va completato entro la 24° settimana
di vita, cioè entro la fine del 6° mese. Il prezzo al
pubblico è di euro 82,90. Entro la fine del 2007 dovrebbe
essere in commercio anche il vaccino della Sanofi Pasteur MSD che
mantiene il nome, con il quale viene indicato negli Stati Uniti, cioè
RotaTeq.
Nell'esposizione
del contenuto di questa pubblicazione mi riferirò, d'ora
innanzi, unicamente al RotaTec.
Le
ragioni per le quali l'AAP raccomanda l'uso di questo vaccino
sono molteplici:
- L'incidenza delle malattie da rotavirus nei Paesi industrializzati e in quelli meno industrializzati sono simili, indicando che la potabilizzazione delle acque e le correnti norme igieniche hanno scarso effetto sulla trasmissione del virus e quindi è difficile che prevengano la malattia;
- Negli Stati Uniti un elevato livello di morbilità da rotavirus continua, nonostante le terapie attualmente disponibili: per esempio la percentuale di ospedalizzazione per gastroenterite nei piccoli bambini si è ridotta solo del 16% dal 1979 al 1995, nonostante l'uso delle soluzioni per la reidratazione orale nel trattamento della disidratazione da gastroenterite;
- Gli studi sull'infezione naturale da rotavirus indicano che la prima infezione protegge il lattante dalle gastroenteriti gravi successive, anche se egli può ancora presentare infezioni asintomatiche e malattie lievi;
- Infine le prove con il vaccino pentavalente contro i rotavirus negli Stati Uniti e in 10 altri Paesi ha mostrato un'efficacia del 98% nel prevenire le malattie gravi e del 74% per prevenire gli episodi di diarrea di qualsiasi entità. Questi risultati sono sovrapponibili a quelli che si riscontrano nel corso della malattia naturale. Per cui la vaccinazione nei primi mesi di vita, che mima l'infezione naturale, non previene tutte le malattie susseguenti, ma previene la maggior parte delle malattie gravi da rotavirus e le loro sequele (come disidratazione, visite mediche e ospedalizzazioni).
Sono in
circolazione molti sierotipi di rotavirus, che causano epidemie di
diarrea dalla fine dell'autunno all'inizio della primavera, al
contrario delle malattie da salmonella, che preferiscono la stagione
calda. I sierotipi sono identificati in base a due proteine di
superficie:
- La glicoproteina VP7 (proteina G), della quale si conoscono 10 sierotipi (da G1 a G10);
- E la proteinaVP4 scissa dalle proteasi (proteina P), che induce la formazione di anticorpi neutralizzanti e della quale si conoscono 11 sierotipi (da P1 a P11).
4 Ceppi
di rotavirus (G1, G3 e G4, combinati con P1A, e G2, combinato con
P1B) sono responsabili del 96% di tutti i ceppi, identificati nel
mondo. Di recente sono emersi altri ceppi, come il G9, in precedenza
molto rari. In una determinata regione i sierotipi predominanti
variano da un anno all'altro.
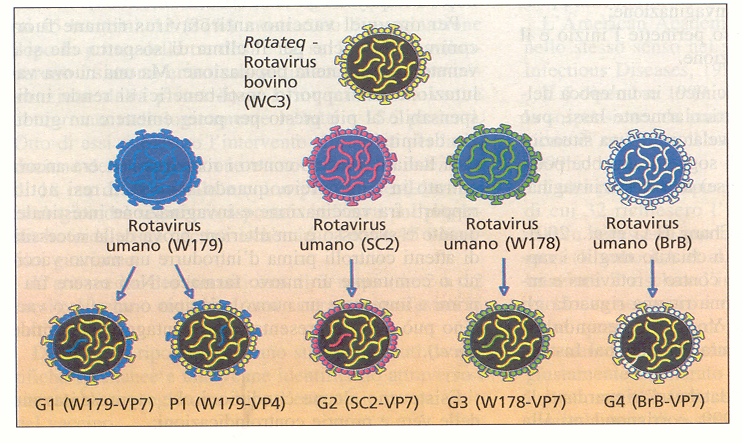
Il
vaccino RotaTeq contiene, in una preparazione orale, 5 rotavirus
riassortiti (riarrangiati) (vedi Figura):
- 4 di loro esprimono una o un'altra delle proteine dell'involucro esterno (G1, G2, G3 e G4), originate da un ceppo di rotavirus umano, riassortiti con la proteina dell'aggancio (P7) originata da un ceppo bovino;
- Il quinto tipo di virus deriva dal riassortimento della proteina (P1A), necessaria per l'aggancio alle cellule, derivata da un ceppo umano, riassortita con un una proteina del capside (G6) derivata da un ceppo bovino di rotavirus
I virus
sono stati coltivati in un terreno costituito da cellule Vero.
Ogni
vaccino contiene: saccarosio, citrato di sodio, fosfato di sodio
monobasico monoidrato, idrossido di sodio, polisorbato 80, terreno
per colture cellulari e tracce di siero di feto bovino.
Il
vaccino non contiene timerosal (tiomersal).
Una
percentuale di sieroconversione per anticorpi IgA verso i rotavirus
fu presente nel 95% di 189 soggetti vaccinati, contro il 14% di 161
soggetti riceventi il placebo (Vesikari T et al, 2006).
Efficacia
del vaccino
L'efficacia
del regime a tre dosi, come abbiamo già visto, è del
74% verso le forme di qualsiasi tipo (gravi e meno gravi) e del 98%
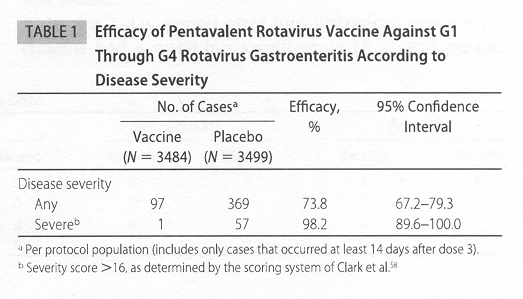
per la gastroenteriti gravi da rotavirus (vedi Tabella 1).

G6
(W179-VP1A)
Tabella
1. Efficacia del vaccino pentavalente contro la gastroenterite da
rotavirus G1-G4 a seconda della gravità della malattia
(Vesikari T e tal, 2006)
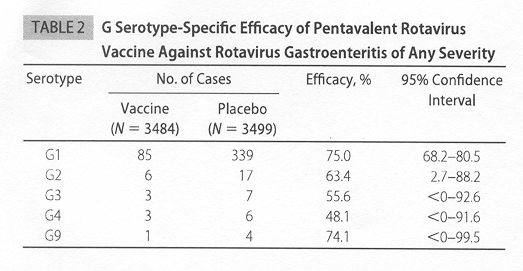
L'efficacia
maggiore è stata dimostrata verso le gastroenterite da
rotavirus G1 (vedi Tabella 2), ma va ricordato che le gastroenteriti
da G1 sono quelle maggiormente frequenti.
Tabella
2. Efficacia del vaccino pentavalente contro i rotavirus nei
confronti di diversi sierotipi di rotavirus e per tutte le gravità
(Vesikari T e tal, 2006)
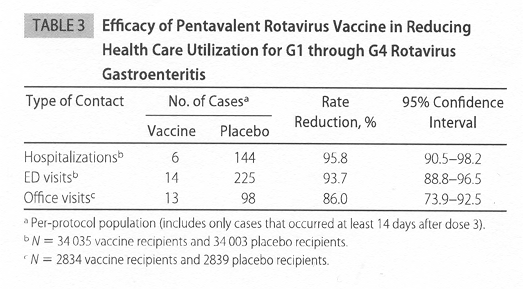
In un
grande studio è stato visto che la vaccinazione contro i
rotavirus riduce dell'86% il numero delle visite in ambulatorio e
del 94% le visite al dipartimento di emergenza. Le ospedalizzazioni
per gastroenterite da rotavirus calarono del 95,8%, mentre le
ospedalizzazioni per ogni tipo di diarrea diminuirono del 59% (vedi
Tabella 3).
Tabella
3. Efficacia del vaccino pentavalente contro i rotavirus nel
ridurre il ricorso all'ospedale per gastroenterite G1-G4 (Vesikari
T e tal, 2006).
Office
visits = visite all'ambulatorio del pediatra
ED =
visite al dipartimento di emergenza dell'ospedale
L'efficacia
del vaccino pentavalente contro i rotavirus nell'anno successivo
alla vaccinazione fu del 63% contro tutte le gastroenteriti da
rotavirus e dell'88% contro quelle gravi (Vesikari T. et al, 2006).
Dati
sull'efficacia della somministrazione di meno di 3 dosi di vaccino
sono molto limitate: la riduzione della ospedalizzazione dopo 1, 2 e
3 dosi fu rispettivamente dell'83%, dell'81% e del 95%.
Né
la somministrazione di latte materno né la co-somministrazione
di altri vaccini sembrò diminuire l'efficacia delle 3 dosi
di vaccino pentavalente. L'efficacia in neonati pretermine (<37
settimane di gestazione) è risultata sovrapponibile, per la
gastroenterite da rotavirus (da G1 a G4) di ogni gravità, a
quella dei lattanti non pretermine (70%), anche se l'intervallo di
confidenza 95% partiva da 0 per il piccolo numero di soggetti presi
in esame.
Sicurezza
del vaccino
Il primo
evento avverso preso in considerazione è stato ovviamente
quello dell'invaginazione, dopo la triste esperienza di qualche
anno fa con il vaccino RRV-TV; per questo il numero dei casi studiati
(> 70.000) è stato così alto nelle due grandi prove
cliniche.
Fra i
soggetti riceventi il vaccino pentavalente non ci furono casi
d'invaginazione confermata nel periodo di 42 giorni dopo la prima
dose, periodo risultato ad alto rischio con il precedente vaccino da
riassortimento umano-scimmia rhesus della Wyeth. Per un periodo di un
anno dopo la prima dose sono stati osservati 13 casi nel gruppo che
aveva ricevuto il vaccino pentavalente della Merck contro 15 caso
d'invaginazione nel gruppo placebo.
L'incidenza
di altri eventi avversi fu simile nel gruppo di vaccinati e nel
gruppo ricevente il placebo. D'altra parte nessun caso di morte,
attribuibile alla vaccinazione, si verificò nel gruppo del
lattanti vaccinati. La più comune causa di morte (17 morti su
un totale di 52) fu la morte improvvisa in culla (SIDS), che fu
ugualmente distribuita fra i soggetti che avevano ricevuto il vaccino
e quelli che avevano ricevuto il placebo (8 e 9 casi
rispettivamente).
Il gruppo
che aveva ricevuto il vaccino presentò nei 42 giorni
successivi alla vaccinazione, un piccolo ma significativo aumento
(p<0,05) di alcuni sintomi in confronto al placebo: vomito (15%
contro 14%), diarrea (24% contro 21%), rino-faringite (7% contro 6%),
otite media (15% contro 13%) e broncospasmo (1,1% contro 0,7%). La
febbre e l'ematochezia furono presenti con la stessa incidenza,
rispettivamente 43% e 0,5%.
Anche nei
soggetti nati pretermine, la vaccinazione con vaccino pentavalente si
è dimostrata sicura.
Diffusione
e trasmissione del ceppi di rotavirus contenuti nel vaccino
I
rotavirus presenti nel vaccino sono stati ritrovati nelle feci dei
bambini vaccinati, da 4 a 6 giorni dopo la vaccinazione, nella
percentuale dell'8,9 dopo la prima dose, ma non furono ritrovati
dopo la seconda dose in 249 bambini vaccinati e vennero ritrovati una
sola volta in 385 bambini dopo la terza dose.
Valutazione
costo-efficacia
La
vaccinazione con 3 dosi del vaccino pentavalente a 2, 4 e 6 mesi,
riduce per un anno, in bambini in età inferiore ai 5 anni:
- di 225.000 le visite da parte del pediatra di famiglia,
- di 137.000 afferenze al dipartimento di emergenza dell'ospedale,
- di 44.000 le ospedalizzazioni e
- di 13 le morti.
Da un
punto di vista unicamente sanitario, la vaccinazione con 3 dosi
(compreso il costo della somministrazione) è utile come
costo-efficacia se la spesa complessiva per bambino è
inferiore ai 66$. Se il costo del vaccino è superiore è
difficile che la vaccinazione sia economicamente vantaggiosa. Con un
prezzo per bambino superiore ai 268 $ un programma d'immunizzazione
contro i rotavirus è facile che rappresenti un costo
aggiuntivo per la società.
Somministrazione
e conservazione del vaccino
Il
vaccino pentavalente contro i rotavirus è contenuto in un tubo
di plastica, facilmente comprimibile, per cui la somministrazione può
essere direttamente praticata nella bocca del bambino. Ogni
confezione contiene una dose da 2 mL di vaccino, in una soluzione
liquida tamponata e stabilizzata, di colore giallo pallido, che può
assumere anche una colorazione rosata. Questa formulazione protegge
il virus del vaccino dall'acidità gastrica e lo stabilizza;
il vaccino va mantenuto a temperatura di frigorifero (+ 2-8°C);
si conserva per 24 mesi. Il vaccino va usato il prima possibile dopo
averlo tolto dal frigorifero.
Controindicazioni
e precauzioni
Il
vaccino pentavalente non va somministrato a lattanti che abbiano una
grave ipersensibilità a un qualsiasi componente del vaccino o
che abbiano presentato una grave reazione allergica a una dose
precedente di vaccino pentavalente contro i rotavirus.
Vanno
considerati i potenziali rischi/benefici di somministrare il vaccino
contro i rotavirus a bambini con alterazioni dell'immunocompetenza
dimostrate o sospette. I bambini e gli adulti con immunodeficienza
congenita o acquisita, trapianto di midollo o di organi solidi, a
volte possono presentare, se vaccinati, gastroenteriti gravi,
prolungate e a volte fatali.
In
generale il vaccino contro i rotavirus deve essere differito di oltre
42 giorni (6 settimane) quando il lattante abbia ricevuto un prodotto
contenente anticorpi: se il differimento di 42 giorni fa sì
che la prima dose del vaccino contro i rotavirus sia data ≥ 13
settimane di età, è necessario ricorrere a un più
breve periodo di tempo per essere sicuri che la prima dose sia data
prima delle 13 settimane di età.
In
situazioni normali, il vaccino pentavalente contro i rotavirus non
deve essere somministrato a bambini con gastroenterite acuta, da
moderata a grave, finché le condizioni generali non
migliorino. I bambini con gastroenterite lieve possono essere
immunizzati, soprattutto quando il ritardo nella vaccinazione
impedisca di vaccinare il lattante prima delle 13 settimane di età.
I pediatri debbono considerare i potenziali rischi e i benefici di
somministrare il vaccino pentavalente contro i rotavirus a lattanti
con preesistenti malattie gastrointestinali: sindromi da
malassorbimento congenito, malattia di Hirschprung, sindrome
dell'intestino corto, vomito persistente di origine sconosciuta.
Lattanti con una storia d'invaginazione possono essere a maggior
rischio di ripetizione dell'episodio, in confronto agli altri
lattanti.
Lattanti
con malattie da moderate a gravi vanno immunizzati non appena siano
guariti dalla fase acuta della malattia.
Per
quanto riguarda i pretermine l'AAP ne consiglia la vaccinazione,
quando siano presenti le seguenti condizioni:
- il lattante abbia almeno 6 settimane di età;
- sia clinicamente stabile;
- il vaccino sia dato alla dimissione o successivamente.
I
lattanti che convivano con persone che abbiano malattie con
immunodeficienza o che presentino alterazioni dello stato immune
possono essere vaccinati: viene consigliato che le persone che
abbiano contatto con le feci di un bambino vaccinato si lavino le
mani accuratamente per almeno una settimana dopo la prima dose del
vaccino contro i rotavirus. Ugualmente il lattante può essere
vaccinato quando conviva con una donna in stato di gravidanza.
Il
pediatra non deve somministrare di nuovo la dose se il lattante abbia
avuto dei rigurgiti o abbia sputato o abbia vomitato durante o dopo
la somministrazione del vaccino. Egli può ricevere le
successive dosi di vaccino agli intervalli raccomandati.
Se il
lattante venisse ospedalizzato per una qualsiasi ragione, dopo la
somministrazione del vaccino, non va presa alcuna precauzione.
Vuoi citare questo contributo?
