Rivista di formazione e aggiornamento di pediatri e medici operanti sul territorio e in ospedale. Fondata nel 1982, in collaborazione con l'Associazione Culturale Pediatri.
Aprile 2005 - Volume VIII - numero 4
M&B Pagine Elettroniche
Pediatria per immagini
I
difetti del tubo neurale
Clinica
Pediatrica, IRCCS, Burlo Garofolo, Trieste
E mail:marzia_lazzerini@libero.it.
Le
immagini sono tratte da un esperienza personale in Brasile
presso l'istituto Materno Infantil de Pernambuco (IMIP).
La
zona del Pernambuco, nel nord-est del Brasile, è tra le
più povere del paese. L'accesso alle cure antenatali
(prevenzione con acido folico, screening con misurazione
dell'alfa-fetoproteina, ecografia fetale) è carente in
particolare per motivi di ordine economico e sociale. Molte
malformazioni rimangono misconosciute sino al momento del parto;
i neonati vengono indirizzati subito dopo la nascita verso
strutture di terzo livello senza che vengano instaurate le
adeguate precauzioni per la prevenzione delle complicazioni
(sovrainfezione). La legislazione brasiliana comunque non
contempla l'interruzione volontaria di gravidanza per i feti
con queste malformazioni.
Per
questi motivi l'incidenza di bambini portatori di
malformazioni gravi è particolarmente elevata, il che
rafforza la necessità di conoscere a fondo l'evoluzione
clinica e le possibilità terapeutiche per la gestione di
questi casi.
I
difetti del tubo neurale (Neural Tube Defects NTDs): Sono
malformazioni risultati da difetti di sviluppo del tubo neurale,
ovvero la struttura embrionaria che si forma per il ripiegamento
e fusione di due estremità della piastra neurale a forma
appunto di tubo, e che dà origine al sistema nervoso
centrale (encefalo e midollo spinale). Comunemente si ritiene
che i difetti del tubo neurale siano secondari a difetti di
fusione (processo che inizia contemporaneamente in segmenti
distinti e che si compie normalmente intorno al 29° giorno
post-concepimento), piuttosto che alla riapertura di segmenti
già precedentemente saldati.
Definizioni:
esiste notevole variabilità nella nomenclatura, comunque
generalmente si definisce quanto segue
Incidenza:
E'
di 1: 1000 nati vivi (negli stadi embrionari l'incidenza è
del 2.5%, la maggio parte esitano in aborti spontanei).
I
difetti più frequenti sono la spina bifida occulta,
l'anencefalia, il mielomeningolcele.
L'incidenza
è lievemente maggiore per il sesso femminile (RR: 1.5), e
per la razza Ispanica, per i figli di madri giovani (<20
anni, RR: 3-4) o particolarmente anziane e per le classi
economiche disagiate.
Il
rischio è maggiore nei figli di madri con diabete
insulino dipendente (sino all'1%).
Il
95% dei bambini con NTDs nascono da coppie senza storia
familiare di questi difetti. Il rischio in una coppia con
parente di primo grado affetto è stimato dello 0.3-4%.
Cause
riconosciute:
Screening
Prenatale:
Gestione:
Anencefalia:
terapia di supporto (mortalità 100% nelle prime 2
settimane).
Encefalocele:
1.
Esame fisico per altre malformazioni (sindrome di Meckel-Gruber)
ed esami strumentali (Eco, Tac, RMN).
2.
Neurochirurgia: da valutare caso per caso in base dimensioni,
sede, qualità del rivestimento cutaneo. Spesso è
necessario uno shunt ventricolo-peritoneale per la compresenza
di idrocefalo (50% dei casi).
3.
Canceling e follow up a lungo termine: i deficit visivi sono
molto comuni negli encefaloceli occipitali. Deficit motori ed
intellettivi dipendono dalla sede e dalle dimensioni della
lesione (>50%).
Mielomeningocele
1.
Esame fisico per malformazioni associate e valutazione
neurologica.
La
valutazione neurologica è importante per determinare il
livello della lesione midollare, da cui dipende in gran parte
l'outcome motorio finale. La presenza dei riflessi sfinterici
suggerisce l'integrità delle vie spinale ed è
prognosticamente importante identificando i bambini a prognosi
migliore .
Tabella
1. CORRELAZIONE TRA SEDE DELLA LESIONE, OBIETTIVITA'
NEUROLOGICA E PROGNOSI SULLA DEAMBULAZIONE.
2.
Cure primarie: Copertura sterile + antibiotici
3.
Valutazione strumentale
4.
Correzione chirurgica: generalmente entro 24-48 h per
scongiurare infezioni
5.
Valutazione complicazioni:
Spina
bifida occulta
Le
rare forme di spina bifida occulta associate a malformazioni
maggiori si rendono evidenti progressivamente se non
diagnosticate nel periodo neonatale con:
La
diagnosi si avvale dell'imaging (RMN). Nelle forme acute il
trattamento chirurgico tempestivo (entro 48h) con decompressione
del midollo spinale può recuperare completamente o
parzialmente la funzionalità.
Tecniche
di chirurgia intrauterina
Per
il mielomeningocele sono attualmente proposte tecniche di
chirurgia intrauterina. Al momento attuale i criteri
internazionalmente accettati per la definizine di candidato
sono: a) mielomeningocele isolato; b) assenza di anomalie
cromosomiche; c) età gestazionale tra le 20 e 25
settimane.
Bibliografia
-
Gomella TL et al- Neonatology. 4° Ed. Lange Medical Books/Mc
Graw Hill 1999.
-
Botto LD, Moore CA, Khoury MJ, Erickson JD. Neural-tube defects.
N Engl J Med 1999;341(20):1509-19.
-
Frey L, Hauser WA. Epidemiology of neural tube defects.
Epilepsia 2003;44 Suppl 3:4-13
-
Sbragia L, Machado IN, Braidos Rojas CE, Zambelli H, Lopes
Miranda M, Bianchi MO, Barini R.. Fetal myelomeningocele and the
potential in-utero repair: follow-up of 58 fetuses. Arq.
Neuro-Psiquiatr. 62 (2) 2004
-
Mitchell LE, Adzick NS, Melchionne J, Pasquariello PS, Sutton
LN, Whitehead AS. Spina bifida. Lancet. 2004;364(9448):1885-95 |
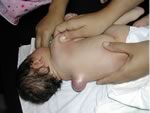
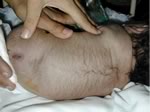
Meningocele
a livello toracico con cute integra.
Il
bambino si presentava senza deficit neurologici
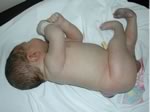
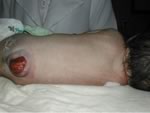
Mielo-meningocele
a livello lombo-sacrale con cute lesa.
E'
evidente il deficit neurologico a livello degli arti inferiori,
con mioatrofia dei segmenti distali e piede torto bilaterale.
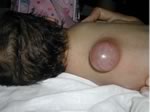
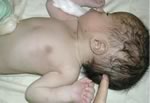
Mielomeningocele
ed idrocefalo.
Bambino
con esposizione di meningi e midollo in sede sacrale.
Era
inoltre presente macrocefalia e diastasi delle suture,
in
un quadro di idrocefalo.
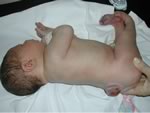
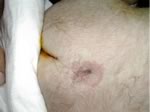
Sospetta
spina bifida occulta.
Bambina
polimalformata (macrosomia, facies particolare, cardiopatia,
piede torto) con seno dermico spinale |
Vuoi citare questo contributo?