Rivista di formazione e aggiornamento di pediatri e medici operanti sul territorio e in ospedale. Fondata nel 1982, in collaborazione con l'Associazione Culturale Pediatri.
Dicembre 2005 - Volume VIII - numero 10
M&B Pagine Elettroniche
Pediatria per l'ospedale
I
meccanismi di azione dei Corticosteroidi
Indirizzo
per la corrispondenza: bartolozzi@unifi.it
L'infiammazione
è una conseguenza dell'infezione: gli agenti infettivi che
superano le barriere epiteliali della cute e delle mucose attivano
direttamente i recettori del complemento e i recettori toll-like, i
due componenti principali del sistema immune innato. Il sistema
immune innato. insieme al sistema immune adattivo, costituisce un
elemento essenziale delle difese dell'individuo nei confronti
dell'infezione: esso rappresenta l'unico sistema di difesa nella
prima settimana dopo l'inizio dell'aggressione batterica, in
attesa che l'immunità adattiva (anticorpi e immunità
cellulare specifica) completi la sua formazione.
L'attivazione della cascata del complemento e dei recettori toll-like porta alla sintesi e alla liberazione dei mediatori dell'infiammazione che hanno un'azione immediata sui capillari e sugli altri piccoli vasi: la vasodilazione localizzata, l'aumentata permeabilità cellulare, la fuoriuscita dai vasi delle proteine plasmatiche e la migrazione dei leucociti nel tessuto colpito dall'infezione, determinano i segni classici dell'infiammazione: calor, dolor, rubor, tumor e functio laesa. Inizia così la produzione di nuove citochine infiammatorie che attivano i leucociti, accorsi nel tessuto interessato dall'infezione. I meccanismi omeostatici anti-infiammatori contrastano con questi processi, contemporaneamente all'eliminazione dell'agente infettivo da parte dell'immunità innata e adattiva. L'asse ipotalamo-ipofisi surrene e in particolare i glicocorticoidi sono essenziali nel limitare e annullare il processo infiammatorio (Rhen T, Cidlowski JA. Antiinfiammatory action of glucocorticoids - New mechanisms for old drugs. N.Engl J Med 2005, 353:1711-23).
I glicocorticoidi, insieme ai mineralocorticoidi, fanno parte dei corticosteroidi: essi costituiscono le due classi di steroidi che vengono sintetizzate fisiologicamente dalla corteccia surrenale. Di norma il corticosurrene sintetizza ogni giorni 10 mg di idrocortisone (cortisolo), di cui la maggior parte nelle ore del mattino o la parte minore nel pomeriggio. Il cortisone, così diffuso in terapia umana, non è sintetizzato dal corticosurrene, cioè esso è un ormone, preparato in periferia a partire dall'idrocortisone.
Nei meccanismi fisiologici del nostro organismo i glicocorticoidi occupano un posto di rilievo in quanto si dimostrano essenziali per controbilanciare gli effetti pro-infiammatori di citochine, chemochine e altri, formati in risposta a un attacco infettivo o di altra natura; la loro azione regolatrice viene quindi ad essere analoga a quella di molti altri sistemi, attivanti e inibenti, presenti negli umani: fattori favorenti la coagulazione e fattori trombolitici, fattori adatti alla digestione endocellulare delle proteine (tripsine) e fattori antitripsina e così via.
Mentre l'infiammazione localizzata è per lo più benefica, l'infiammazione eccessiva o persistente può portare alla distruzione di tessuto e alla malattia. Insieme ad altri disordini, come l'asma e altre malattie allergiche, le malattie autoimmunitarie e le sepsi, essa è una causa importante di malattia e di morte. I glicocorticoidi sono indicati per la maggior parte di queste affezioni; la loro efficacia nel curare i disordini infiammatori deriva dall'effetto pleiotropico del recettore dei glicocorticoidi su una molteplicità di vie metaboliche. Ma questo effetto molteplice dei glicocorticoidi può determinare, oltre agli effetti favorevoli, anche degli effetti contrari, come il ritardo di crescita nei bambini, l'immunosoppressione, l'ipertensione, l'inibizione della guarigione delle ferite, l'osteoporosi e le alterazioni metaboliche. Tutte queste attività possono alla lunga divenire pericolose per l'organismo, per cui esse complessivamente controindicano l'uso prolungato dei glicocorticoidi.
Di seguito verranno presi in considerazione i meccanismi, con i quali i glicocorticoidi inibiscono l'infiammazione e insieme le limitazione di questi ormoni in terapia.
L'attivazione della cascata del complemento e dei recettori toll-like porta alla sintesi e alla liberazione dei mediatori dell'infiammazione che hanno un'azione immediata sui capillari e sugli altri piccoli vasi: la vasodilazione localizzata, l'aumentata permeabilità cellulare, la fuoriuscita dai vasi delle proteine plasmatiche e la migrazione dei leucociti nel tessuto colpito dall'infezione, determinano i segni classici dell'infiammazione: calor, dolor, rubor, tumor e functio laesa. Inizia così la produzione di nuove citochine infiammatorie che attivano i leucociti, accorsi nel tessuto interessato dall'infezione. I meccanismi omeostatici anti-infiammatori contrastano con questi processi, contemporaneamente all'eliminazione dell'agente infettivo da parte dell'immunità innata e adattiva. L'asse ipotalamo-ipofisi surrene e in particolare i glicocorticoidi sono essenziali nel limitare e annullare il processo infiammatorio (Rhen T, Cidlowski JA. Antiinfiammatory action of glucocorticoids - New mechanisms for old drugs. N.Engl J Med 2005, 353:1711-23).
I glicocorticoidi, insieme ai mineralocorticoidi, fanno parte dei corticosteroidi: essi costituiscono le due classi di steroidi che vengono sintetizzate fisiologicamente dalla corteccia surrenale. Di norma il corticosurrene sintetizza ogni giorni 10 mg di idrocortisone (cortisolo), di cui la maggior parte nelle ore del mattino o la parte minore nel pomeriggio. Il cortisone, così diffuso in terapia umana, non è sintetizzato dal corticosurrene, cioè esso è un ormone, preparato in periferia a partire dall'idrocortisone.
Nei meccanismi fisiologici del nostro organismo i glicocorticoidi occupano un posto di rilievo in quanto si dimostrano essenziali per controbilanciare gli effetti pro-infiammatori di citochine, chemochine e altri, formati in risposta a un attacco infettivo o di altra natura; la loro azione regolatrice viene quindi ad essere analoga a quella di molti altri sistemi, attivanti e inibenti, presenti negli umani: fattori favorenti la coagulazione e fattori trombolitici, fattori adatti alla digestione endocellulare delle proteine (tripsine) e fattori antitripsina e così via.
Mentre l'infiammazione localizzata è per lo più benefica, l'infiammazione eccessiva o persistente può portare alla distruzione di tessuto e alla malattia. Insieme ad altri disordini, come l'asma e altre malattie allergiche, le malattie autoimmunitarie e le sepsi, essa è una causa importante di malattia e di morte. I glicocorticoidi sono indicati per la maggior parte di queste affezioni; la loro efficacia nel curare i disordini infiammatori deriva dall'effetto pleiotropico del recettore dei glicocorticoidi su una molteplicità di vie metaboliche. Ma questo effetto molteplice dei glicocorticoidi può determinare, oltre agli effetti favorevoli, anche degli effetti contrari, come il ritardo di crescita nei bambini, l'immunosoppressione, l'ipertensione, l'inibizione della guarigione delle ferite, l'osteoporosi e le alterazioni metaboliche. Tutte queste attività possono alla lunga divenire pericolose per l'organismo, per cui esse complessivamente controindicano l'uso prolungato dei glicocorticoidi.
Di seguito verranno presi in considerazione i meccanismi, con i quali i glicocorticoidi inibiscono l'infiammazione e insieme le limitazione di questi ormoni in terapia.
Azioni
basilari dei glicocorticoidi endogeni
L'asse
ipotalamo-ipofisi-surrene gioca un ruolo centrale nel regolare i
segnali sui recettori dei glicocorticoidi, presenti praticamente su
tutte le cellule. In breve, segnali nervosi, endocrini e citochimici
convergono a livello del nucleo periventricolare dell'ipotalamo per
controllare la secrezione dell'ormone liberante la corticotropina
(ACTH) nel sistema portale ipofisario. Ne consegue che la liberazione
dell'ormone liberante la corticotropina porta alla liberazione di
ACTH da parte dell'ipofisi anteriore. L'ACTH induce a sua volta
la sintesi e la secrezione di idrocortisone (cortisolo) da parte
della corteccia surrenale. La maggior parte del cortisolo secreto
(circa il 90%) è legato alle globuline, leganti i
corticosteroidi, nel sangue circolante. Il cortisolo libero è
la parte biologicamente attiva dell'ormone ed è convertito a
cortisone dalla 11-_-idrossisteroido-deidrogenasi, tipo 2. Al
contrario il tipo 1 di 11-_-idrossisteroido-deidrogenasi converte il
cortisone in idrocortisone.
Il recettore dei glicocorticoidi è un membro della famiglia delle proteine che legano gli ormoni steroidei. Esso si lega fortemente all'idrocortisone e promuove il distacco dai recettori degli “chaperon” molecolari, incluse le proteine heat-shock.
Il recettore dei glicocorticoidi è un membro della famiglia delle proteine che legano gli ormoni steroidei. Esso si lega fortemente all'idrocortisone e promuove il distacco dai recettori degli “chaperon” molecolari, incluse le proteine heat-shock.
All'interno
della cellula l'idrocortisone agisce in tre modi:
- il complesso recettore-cortisolo muove verso il nucleo, dove si lega, come un omodimero (un complesso di due proteine identiche, legate da un ponte non covalente), alle sequenze del DNA, chiamate elementi glucocorticoidi-respondenti. Il risultante complesso agisce come attivatore o repressore di proteine che iniziano la trascrizione di alcuni geni da parte della RNA polimerasi II.
- la stimolazione di altri geni riguarda l'interazione fra il complesso recettore-cortisolo e altri fattori di trascrizione, come il fattore-kB. Questa ultima azione avviene a bassi livelli di cortisolo.
- il terzo meccanismo interessa i recettori, presenti sulla membrana cellulare e un secondo messaggero, chiamato “via non genomica”, perché agisce attraverso la stimolazione di parti, non corrispondenti a componenti nucleari.
I
glicocorticoidi quindi inibiscono l'infiammazione attraverso questi
3 meccanismi, di cui due legati a effetti diretti e indiretti su
alcuni geni, presenti nel nucleo della cellula, e uno dovuto a un
effetto non legato ai geni (non genomico) (vedi figura
1 e figura
2).
Struttura
del recettore dei glicocorticoidi
Il gene
del recettore umano dei glicocorticoidi (GR) è un locus del
cromosoma 5q31-32 (figura
3). Le variazioni nella struttura e nella espressione di questo
gene portano a modificazioni nel segnale dei glicocorticoidi, per cui
modificazioni nei diversi componenti di questo gene portano a dirette
conseguenze sull'attività dei glicocorticoidi.
Regolazione
neuroendocrina dell'infiammazione
L'interazione
fra sistema nervoso, asse ipotalamo-ipofiso-surrene e componenti del
sistema immune innato e adattivo, gioca un ruolo chiave nella
regolazione dell'infiammazione e della immunità. Per esempio
le citochine e i mediatori dell'infiammazione attivano i recettori
periferici del dolore, i cui assoni attraverso le corna dorsali del
midollo e le sinapsi con il tratto lemniscale, portano il segnale del
dolore al talamo e alla corteccia somato-sensitiva. L'attivazione
di questa via nocicettiva stimola infine l'attività
dell'asse ipotalamo-ipofisi-surrene.
I glicocorticoidi, che vengono così sintetizzato, inibiscono a loro volta la sintesi di citochine e di mediatori dell'infiammazione, venendo così a formare un ansa feedback negativa. Le citochine possono agire anche sul cervello, attivando direttamente l'asse diencefalo-ipofisi-surrene. Una cattiva regolazione di questa ansa neuroendocrina determina modificazioni generali nell'infiammazione e nell'immunità.
L'iperattività dell'asse ipotalamo-ipofisi-surrene in assenza d'infiammazione, come avviene nella sindrome di Cushing, determina immunosoppressione e aumenta quindi la suscettibilità alle infezioni. Il dolore fisico, il trauma emotivo e la restrizione calorica attivano l'asse ipotalamo-ipofisi-surrene e causano immunosoppressione. Anche la diminuzione dell'attività dell'asse ipotalamo-ipofisi-surrene e bassi livelli di glicocorticoidi aumentano la suscettibilità alle infezioni e la gravità stessa dell'infiammazione. I pazienti con malattia di Addison, per esempio, necessitano della somministrazione di glicocorticoidi durante le infezioni e l'infiammazione per prevenire l'effetto dannoso delle citochine. La cattiva regolazione dell'asse ipotalamo-ipofisi-surrene da parte dell'infiammazione si associa a una cattiva prognosi in pazienti con sindrome da difficoltà respiratoria acuta. Analogamente la resistenza acquisita ai corticosteroidi è un evento comune nei pazienti con artrite reumatoide cronica per una diminuita espressione del recettore _ dei glicocorticoidi, per un'aumentata espressione del recettore _ o per in attivazione della chinasi proteica attivata dai fitogeni (MAPK), che fosforilizza il recettore dei glicocorticoidi e inibisce quindi la capacità segnalante di questi ormoni.
I glicocorticoidi, che vengono così sintetizzato, inibiscono a loro volta la sintesi di citochine e di mediatori dell'infiammazione, venendo così a formare un ansa feedback negativa. Le citochine possono agire anche sul cervello, attivando direttamente l'asse diencefalo-ipofisi-surrene. Una cattiva regolazione di questa ansa neuroendocrina determina modificazioni generali nell'infiammazione e nell'immunità.
L'iperattività dell'asse ipotalamo-ipofisi-surrene in assenza d'infiammazione, come avviene nella sindrome di Cushing, determina immunosoppressione e aumenta quindi la suscettibilità alle infezioni. Il dolore fisico, il trauma emotivo e la restrizione calorica attivano l'asse ipotalamo-ipofisi-surrene e causano immunosoppressione. Anche la diminuzione dell'attività dell'asse ipotalamo-ipofisi-surrene e bassi livelli di glicocorticoidi aumentano la suscettibilità alle infezioni e la gravità stessa dell'infiammazione. I pazienti con malattia di Addison, per esempio, necessitano della somministrazione di glicocorticoidi durante le infezioni e l'infiammazione per prevenire l'effetto dannoso delle citochine. La cattiva regolazione dell'asse ipotalamo-ipofisi-surrene da parte dell'infiammazione si associa a una cattiva prognosi in pazienti con sindrome da difficoltà respiratoria acuta. Analogamente la resistenza acquisita ai corticosteroidi è un evento comune nei pazienti con artrite reumatoide cronica per una diminuita espressione del recettore _ dei glicocorticoidi, per un'aumentata espressione del recettore _ o per in attivazione della chinasi proteica attivata dai fitogeni (MAPK), che fosforilizza il recettore dei glicocorticoidi e inibisce quindi la capacità segnalante di questi ormoni.
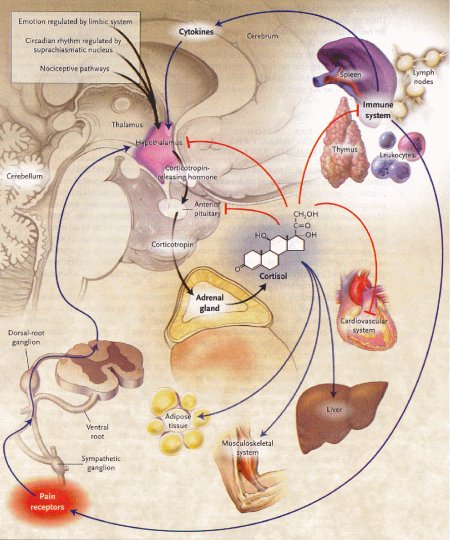
Figura
1 – Vie di comunicazione fra il sistema nervoso, l'asse
ipotalamo-ipofisi-surrene e altri tessuti, influenzati dai segnali
dei corticosteroidi.
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)

Le
frecce rosse dimostrano inibizione e le frecce blu o nere indicano
attivazione.
Meccanismi
antiinfiammatori di segnalazione
I
glicocorticoidi e i loro recettori sono situati all'apice di una
rete regolatoria che blocca molte vie infiammatorie (vedi figura 4).
Per esempio i glicocorticoidi possono inibire la produzione di
prostaglandine attraverso tre meccanismi indipendenti:
- induzione e attivazione dell'annessina 1
- induzione della fosfatasi 1 MAPK
- repressione della trascrizione della cicloossigenasi 2.
Figura
2 – I tre principali meccanismi di azione dei glicocorticoidi e dei
suoi recettori nell'inibizione dell'infiammazione.
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)
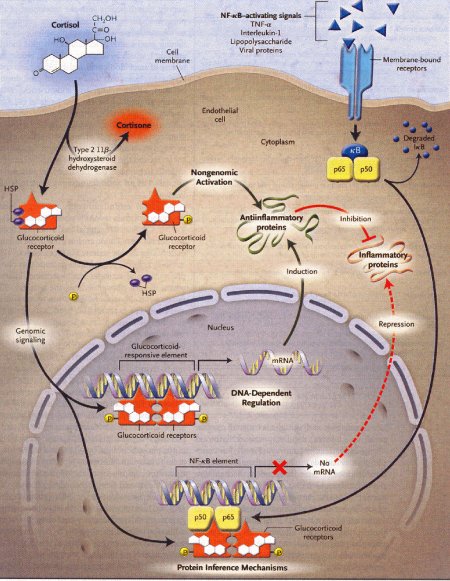
TNF-_ =
tumor necrosis factor _
HSP = heat-shock protein
mRNA = RNA messaggero
P = fosfati
Le frecce nere indicano attivazione, le frecce rosse invece inibizione, il segno X indica mancanza di produzione (blocco), cioè non produzione di mRNA.
HSP = heat-shock protein
mRNA = RNA messaggero
P = fosfati
Le frecce nere indicano attivazione, le frecce rosse invece inibizione, il segno X indica mancanza di produzione (blocco), cioè non produzione di mRNA.
Figura
3 – Localizzazione del gene e organizzazione del recettore umano
per i glicocorticoidi (GR).
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)
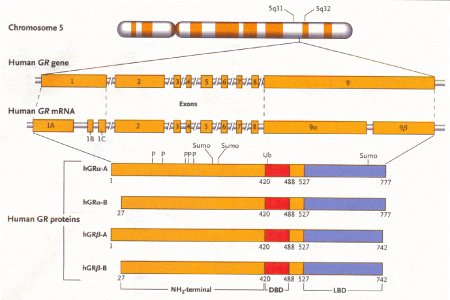
La
diversità nella espressione e nella funzione dei recettori dei
glicocorticoidi risulta dalla sede alternativa della
trascrizione.
DBP = indica il dominio legante il DNA
LBD = indica il dominio legante il ligando
hGR = recettore umano dei glicocorticoidi
DBP = indica il dominio legante il DNA
LBD = indica il dominio legante il ligando
hGR = recettore umano dei glicocorticoidi
L'
annessina 1 (chiamata anche lipocortina-1) è una proteina
anti-infiammatoria che fisicamente interagisce e inibisce una
fosfolipasi citosolica A2_ (cPLA2_). Questa
proteina legante il calcio richiede elevati livelli di calcio e
l'azione di fosforilazione da parte della proteinchinasi MAPK. II
calcio/calmodulina dipendente e la chinasi MAPK sono infatti
necessari perché essa eserciti la sua attività
enzimatica. L'attivazione della cPLA2 _ da parte dello
stimolo infiammatorio inizia al momento della fosforilazione da parte
del citosol sulla membrana perinucleare, dove esso idrolizza i
fosfolipidi contenenti acido arachidonico. I glicocorticoidi inducono
e attivano l'annessina 1, che, inibendo la cPLA2_,
blocca la liberazione di acido arachinonico e la sua successiva
conversione in acido eicosanoide (cioè prostaglandine,
tromboxani, prostracicline e leucotrieni). I topi, mancanti di
annessina 1 hanno elevati livelli di cPLA2_ , un'esagerata
risposta infiammatoria e una resistenza parziale all'azione
anti-infiammatoria dei glicocorticoidi. Esiste una forte correlazione
fra livelli di cortisolo basali, stimolati da parte dell'ACTH da un
lato e l'espressione dell'annessina 1 sui neutrofili umani
dall'altro; è sconosciuta l'importanza clinica
dell'annessina 1 come proteina anti-infiammatoria.
Una seconda proteina anti-infiammatoria, indotta dai glicocorticoidi è la fosfatasi 1 MAPK. Le citochine, le infezioni batteriche e virali e la luce ultravioletta sono alcuni segnali infiammatori che attivano la cascata MAPK. La fosfatasi MAPK defosforila e inattiva tutti i membri della famiglia delle proteine MAPK, inclusa la chinasi Jun N-terminale, le chinasi 1 e 2, dei segnali extracellulari, e la chianasi p38. Di conseguenza la fosfatasi 1 MAPK può inibire anche l'attività cPLA2_ bloccando la fosforilazione da parte della chinasi MAPK e MAPK interagente. Inoltre i glicocorticoidi e il loro recettore interferiscono direttamente con la trascrizione c-Jun mediata.
Una seconda proteina anti-infiammatoria, indotta dai glicocorticoidi è la fosfatasi 1 MAPK. Le citochine, le infezioni batteriche e virali e la luce ultravioletta sono alcuni segnali infiammatori che attivano la cascata MAPK. La fosfatasi MAPK defosforila e inattiva tutti i membri della famiglia delle proteine MAPK, inclusa la chinasi Jun N-terminale, le chinasi 1 e 2, dei segnali extracellulari, e la chianasi p38. Di conseguenza la fosfatasi 1 MAPK può inibire anche l'attività cPLA2_ bloccando la fosforilazione da parte della chinasi MAPK e MAPK interagente. Inoltre i glicocorticoidi e il loro recettore interferiscono direttamente con la trascrizione c-Jun mediata.
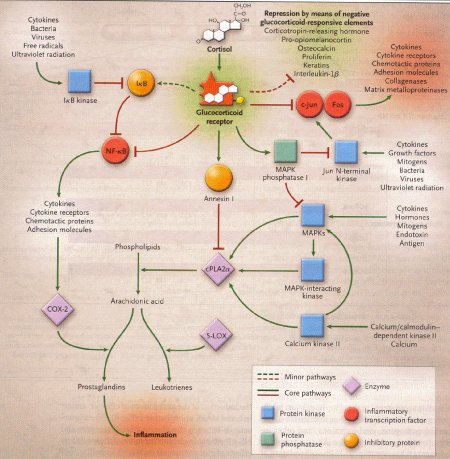
Figura
4 –Architettuta molecolare parziale riguardante l'antagonismo dei
glicocorticoidi con l'infiammazione
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)
(fonte: Rhen T, Cidlowski JA. N.Engl J Med 2005, 353:1711-23)

Le vie
infiammatorie sono caratterizzate da anse feedback positive.I
recettori dei glicocorticoidi inibiscono queste vie in diversi punti
sia bloccando la trascrizione delle proteine infiammatorie da parte
dell'NF-_B e proteina 1 attivatrice, sia inducendo l'espressione
di proteine anti-infiammatorie, come _B1, annessina 1 e fosfatasi 1
MAPK.
5-LOX = 5-lipodssigenasi; COX-2 = cicloossigenasi 2. Le linee rosse significano inibizione e le frecce rosse attivazione.
5-LOX = 5-lipodssigenasi; COX-2 = cicloossigenasi 2. Le linee rosse significano inibizione e le frecce rosse attivazione.
Il
complesso del recettore del cortisolo interagisce anche fisicamente
con il NF-_B per bloccare la sua attività trascrizionale. Nel
suo stato inattivo NF-_B è sequestrato nel citoplasma da una
proteina inibitoria, chiamata I_B. Il tumor necrosis factor _,
l'interleuchina 1, gli agenti microbici, le infezioni virali e
altri stimoli infiammatori attivano la cascata che attiva le chinasi
I_B. La fosforilazione dell'I_B porta alla sua degradazione da
parte del proteasoma e alla liberazione dell'NF-_B. Nel nucleo,
l'NF-_B si lega alle sequenze del DNA, chiamate elementi NF-_B e
stimola la trascrizione delle citochine, delle chemochine, delle
molecole di adesione cellulare, dei fattori del complemento e dei
recettori di queste molecole. L'NF-_B induce inoltre la
trascrizione della ciclossigenasi 2, un enzima essenziale per la
produzione di prostaglandine. Così l'antagonismo del NF-_B,
indotto dai glicorticoidi, e la repressione della ciclossigenasi 2
rappresentano un ulteriore meccanismo d'inibizione della sintesi
delle prostaglandine, dopo l'induzione degli antagonisti del
cPLA2_, da parte dell'annessina 1 e della fosfatasi 1 MAPK (vedi
figura 4). L'interazione diretta fra recettore dei
glicocorticoidi e NF-_B probabilmente riguarda la maggior parte degli
effetti inibitori dei glicocorticoidi sull'azione segnalante del
NF-_B. I glicocorticoidi e i recettori dei glicocorticoidi modulano
anche l'attività di altri fattori di trascrizione.
Recenti pubblicazioni suggeriscono che i glicocorticoidi possono avere un rapido effetto sull'infiammazione, anche senza determinare cambiamenti nell'espressione dei geni. Il meccanismo non genomico, meglio descritto, interessa l'attivazione della sintetasi dell'ossido nitrico endoteliale (eNOS). I glicocorticoidi stimolano l'attività della fosfatidilinositol-3-idrossichinasi (PI3K) in un recettore corticoido-dipendente, ma non trascrizione-indipendente, presente sulle cellule endoteliali umane. L'attivazione del PI3K porta alla fosforilazione dell'Akt. L'Akt fosforilato fosforilizza e attiva eNOS, con la conseguente produzione di ossido nitrico. Questo reperto è sorprendente perché la produzione di ossido nitrico è generalmente associata a vasodilatazione e infiammazione. Molte ricerche saranno necessarie per chiarire il ruolo dei meccanismi non-transcrizionali nell'inibizione della vasodilatazione, della permeabilità vascolare e della migrazione dei leucociti attraverso l'endotelio.
Risulta evidente da tutto questo che i glicocorticoidi agiscono a diversi livelli mediante meccanismi multipli per controllare l'infiammazione.
Recenti pubblicazioni suggeriscono che i glicocorticoidi possono avere un rapido effetto sull'infiammazione, anche senza determinare cambiamenti nell'espressione dei geni. Il meccanismo non genomico, meglio descritto, interessa l'attivazione della sintetasi dell'ossido nitrico endoteliale (eNOS). I glicocorticoidi stimolano l'attività della fosfatidilinositol-3-idrossichinasi (PI3K) in un recettore corticoido-dipendente, ma non trascrizione-indipendente, presente sulle cellule endoteliali umane. L'attivazione del PI3K porta alla fosforilazione dell'Akt. L'Akt fosforilato fosforilizza e attiva eNOS, con la conseguente produzione di ossido nitrico. Questo reperto è sorprendente perché la produzione di ossido nitrico è generalmente associata a vasodilatazione e infiammazione. Molte ricerche saranno necessarie per chiarire il ruolo dei meccanismi non-transcrizionali nell'inibizione della vasodilatazione, della permeabilità vascolare e della migrazione dei leucociti attraverso l'endotelio.
Risulta evidente da tutto questo che i glicocorticoidi agiscono a diversi livelli mediante meccanismi multipli per controllare l'infiammazione.
Limitazioni
della terapia con glicocorticoidi
Mentre i
benefici immediati del trattamento con corticosteroidi derivano da
modificazioni vascolari di breve durata e da una limitata
immunosoppressione, il trattamento con glicocorticoidi di lunga
durata o con dosi elevate ha molti effetti collaterali (vedi tabella
2).
Tabella
2 – Effetti collaterali specifici di tessuto, in seguito all'uso
di dosi alte e prolungate di glicocorticoidi
Tessuto | Effetti
collaterali |
Surrene | Atrofia
surrrenalica. Sindrome di Cushing |
Sistema
cardio-vascolare | Displipidemia,
ipertensione, trombosi, vasculite |
Sistema
nervoso centrale | Modificazioni
del comportamento, dell'apprendimento, della memoria e
dell'umore (cioè psicosi), atrofia cerebrale |
Apparato
gastro-intestinale | Sanguinamento
gastro-intestinale, pancreatine, ulcera peptica |
Sistema
immune | Ampia
immunosoppressione, attivazione di virus latenti, |
Cute | Atrofia,
guarigione ritardata delle ferite, eritema, ipertrricosi,
dermatite periorale, petecchie, acne indotta dai glicocorticoidi,
strie rubre, teleangectasie |
Sistema
muscolo-scheletrico | Necrosi
ossea, atrofia muscolare, osteoporosi, ritardo di crescita
longitudinale delle ossa |
Occhi | Cataratta,
glaucoma |
Rene | Aumentata
ritenzione di sodio e aumentata escrezione di potassio |
Sistema
riproduttivo | Pubertà
ritardata, ritardo di crescita fetale, ipogonsadismo |
Il
trattamento prolungato con glicocorticoidi può causare
ipertensione attraverso due meccanismi:
- la ritenzione renale di sodio e quindi l'aumento del volume ematico
- il potenziamento delle risposte vasopressorie all'angiotensina II e alle catecolamine.
L'aumentata
risposta all'angiotensina II è dovuta all'induzione dei
suoi recettori da parte dei glicocorticoidi. D'altra parte i
glicocorticoidi non modificano il numero o l'affinità dei
recettori _1-adrenergici, mentre invece potenziano i
segnali _1-adrenergici.
Sebbene
la resistenza vascolare sistemica, indotta dai glicocorticoidi, sia
dannosa, modificazioni localizzate nella vasoreattività
possono portare a effetti benefici con il trattamento combinato,
glicocorticoidi + _2-agonisti, nei pazienti con asma. Un
corso di due settimane di glicocorticoidi inalati infatti diminuisce
la perfusione basale della mucosa polmonare e ristabilisce la
risposta vascolare ai _2-agonisti in pazienti con asma.
La
crescita longitudinale nei bambini è il risultato della
proliferazione e differenziazione dei condrociti e la successiva
ossificazione della matrice extracellulare nelle placche di crescita
delle ossa lunghe. Le cellule staminali risiedono all'estremo
epifisario del piatto delle ossa lunghe e danno luogo alla
proliferazione dei condrociti. Quanto più si allontanano
dall'osso metafisario e quanto più i condrociti rallentano
la loro velocità di proliferazione, iniziano a ipertrofizzarsi
e producono le proteine della matrice extracellularre e le
metalloproteinasi della matrice. Mentre i condrociti preparano questa
impalcatura, essi assorbono calcio e secernono fosfato e
idrossiapatite. Infine essi vanno incontro ad apoptosi lasciando
dietro di loro l'osso mineralizzato. I glicocorticoidi rallentano
la crescita longitudinale riducendo la proliferazione dei condrociti
e determinando l'apoptosi di queste cellule. L'inibizione del
fattore 1 di crescita, insulino-simile, è uno dei meccanismi
attraverso i quali si manifesta la riduzione dei condrociti. Il
fattore 1 di crescita insulino-simile aumenta la fosforilazione
dell'AKT e agisce come un fattore di sopravvivenza dei condrociti
trattati con glicocorticoidi. Sebbene vi possa essere una ripresa
della crescita quando il trattamento corticosteroideo viene sospeso,
trattamenti prolungati durante l'infanzia e la fanciullezza spesso
si associano a diminuzione della statura dell'adulto.
I glicocorticoidi hanno un effetto deleterio anche sull'osso dell'adulto. Osteoporosi e aumentato rischio di fratture sono i principali effetti collaterali del trattamento con glicocorticoidi. L'osteoporosi in risposta ai glicocorticoidi è dovuta in parte all'inibizione della trascrizione della osteocalcina negli osteoblasti; l'osteocalcina è un'importante proteina della matrice extracellulare, che promuove la mineralizzazione delle ossa.
Riassumendo i glicocorticoidi aggravano l'osteoporosi inducendo l'apoptosi degli osteoblasti e aumentando l'attività degli osteoclasti.
I glicocorticoidi inibiscono anche la guarigione delle lesioni asettiche. Per esempio le fratture inducono l'infiammazione, mentre la produzione di citochine si ritiene sia essenziale per la guarigione e il rimodellamento dell'osso. Oltre a bloccare la sintesi delle citochine, i gloicocorticoidi inibiscono la sintesi delle metalloproteinasi e del collageno della matrice, fattori importanti per la guarigione delle ferite.
Inoltre i glicocorticoidi promuovono la gliconeogenesi nel fegato, la degradazione delle proteine in aminoacidi nel muscolo (atrofia) e la lipolisi. Non ci sono al momento mezzi per migliorare gli effetti collaterali della terapia prolungata con corticosterodi, sia a livello dei recettori che degli elementi steroidi.-responsivi. Spesso viene usato un trattamento con insulina per un diabete indotto dai glicocosrticoidi o con bifosfonati per l'osteoporosi.
L'esistenza di questi problemi ha indotto i ricercatori a identificare glicocorticoidi potenzialmente selettivi.
I glicocorticoidi hanno un effetto deleterio anche sull'osso dell'adulto. Osteoporosi e aumentato rischio di fratture sono i principali effetti collaterali del trattamento con glicocorticoidi. L'osteoporosi in risposta ai glicocorticoidi è dovuta in parte all'inibizione della trascrizione della osteocalcina negli osteoblasti; l'osteocalcina è un'importante proteina della matrice extracellulare, che promuove la mineralizzazione delle ossa.
Riassumendo i glicocorticoidi aggravano l'osteoporosi inducendo l'apoptosi degli osteoblasti e aumentando l'attività degli osteoclasti.
I glicocorticoidi inibiscono anche la guarigione delle lesioni asettiche. Per esempio le fratture inducono l'infiammazione, mentre la produzione di citochine si ritiene sia essenziale per la guarigione e il rimodellamento dell'osso. Oltre a bloccare la sintesi delle citochine, i gloicocorticoidi inibiscono la sintesi delle metalloproteinasi e del collageno della matrice, fattori importanti per la guarigione delle ferite.
Inoltre i glicocorticoidi promuovono la gliconeogenesi nel fegato, la degradazione delle proteine in aminoacidi nel muscolo (atrofia) e la lipolisi. Non ci sono al momento mezzi per migliorare gli effetti collaterali della terapia prolungata con corticosterodi, sia a livello dei recettori che degli elementi steroidi.-responsivi. Spesso viene usato un trattamento con insulina per un diabete indotto dai glicocosrticoidi o con bifosfonati per l'osteoporosi.
L'esistenza di questi problemi ha indotto i ricercatori a identificare glicocorticoidi potenzialmente selettivi.
Glicorticoidi
selettivi e terapie del futuro.
E'
ormai chiaro che gli effetti anti-infiammatori dei glicocorticoidi
sono principalmente mediati dall'inibizione dell'NF-_B e della
proteina 1 attivatrice, mentre i loro effetti collaterali derivano
dall'attivazione della trascrizione.
Uno studio recente (Schacke H et al, Proc Nat Acad Sci USA 2004, 101:227-32) ha descritto un nuovo cortisonico (ZK216348) con un quadro di repressione e attivazione della trascrizione, che è risultato dranmaticamente differente da quello dei vecchi glicocorticoidi. Il livello di glicocorticoide richiesto per reprimere l'interleuchina 8 nei monociti è da 8 a 12 volte superiore, quello richiesto per indurre la tiroxina.-aminotranferasi nelle cellule epatiche.
Esiste quindi la possibilità di sviluppare selettivi glicocorticoidi dotati di un migliore profilo terapeutico.
Uno studio recente (Schacke H et al, Proc Nat Acad Sci USA 2004, 101:227-32) ha descritto un nuovo cortisonico (ZK216348) con un quadro di repressione e attivazione della trascrizione, che è risultato dranmaticamente differente da quello dei vecchi glicocorticoidi. Il livello di glicocorticoide richiesto per reprimere l'interleuchina 8 nei monociti è da 8 a 12 volte superiore, quello richiesto per indurre la tiroxina.-aminotranferasi nelle cellule epatiche.
Esiste quindi la possibilità di sviluppare selettivi glicocorticoidi dotati di un migliore profilo terapeutico.
Conclusioni
Gli
effetti anti-infiammatori e immunosoppressivi dei glicocorticoidi
utilizzano molti meccanismi molecolari, che sono stati chiariti
grazie alla ricerca di base.
Come abbiamo visto tre meccanismi principali riguardano gli effetti dei corticosteroidi:
Come abbiamo visto tre meccanismi principali riguardano gli effetti dei corticosteroidi:
- il legame dei cortocosterodi ai recettori, localizzati sugli elementi glicocorticoidi-responsivi (come l'induzione dell'annessina 1 e della MAPK fosfatasi 1),
- gli effetti indiretti sull'espressione dei geni, attraverso l'interazione dei recettori dei glicocorticoidi su altri fattori di trascrizione (cioè NF-_B e attivatore della proteina 1)
- e gli effetti (non-genomici) mediati dai recettori dei glicocorticoidi sulla cascata del secondo messaggero (cioè la via PI3K-Akt-eNOS).
Sfortunatamente
poiché alcuni di questi meccanismi sono interessati anche ai
segnali fisiologici, oltre che ai segnali anti-infiammatori, gli
effetti terapeutici dei glicocorticoidi sull'infiammazione si
accompagnano spesso a significativi effetti collaterali.
E'
augurabile che si arrivi alla preparazione di glicocorticoidi
provvisti di affetti benefici, senza presentare gli effetti
sfavorevoli (Buttgereit et al. Lancet 2005, 365:801-3).
Vuoi citare questo contributo?
