Gennaio 2010 - Volume XIII - numero 1
M&B Pagine Elettroniche
Contributi Originali - Casi contributivi
Una
gambina più grossa
1Medico-chirurgo,
2Pediatra di Famiglia, Napoli
Indirizzo
per corrispondenza: mayer.marina@libero.it
A
childs larger leg
Key
words
Isolated
hemihyperplasia, Lower limb disporprotion, Cancer risk, Follow
up
Summary
The
Authors describe a case of isolated hemihyperplasia (HHI)
diagnosed on a three-month-old female child. During a visit at
our pediatric surgery disproportion of the limbs was noticed, so
the child was sent to genetic counselling. HHI diagnosis, as a
result of an increased cancer risk, requires a regular follow-up
until end of development. |
|
Riassunto
Descriviamo
un caso di emiiperplasia isolata (EII) diagnosticata ad una
bambina di tre mesi. Ad una visita di controllo presso il nostro
ambulatorio pediatrico abbiamo evidenziato la sproporzione degli arti
e abbiamo inviato la piccola a effettuare una consulenza genetica. La
diagnosi di EII, a causa di un incrementato rischio oncologico,
richiede un follow-up periodico sino a sviluppo ultimato.
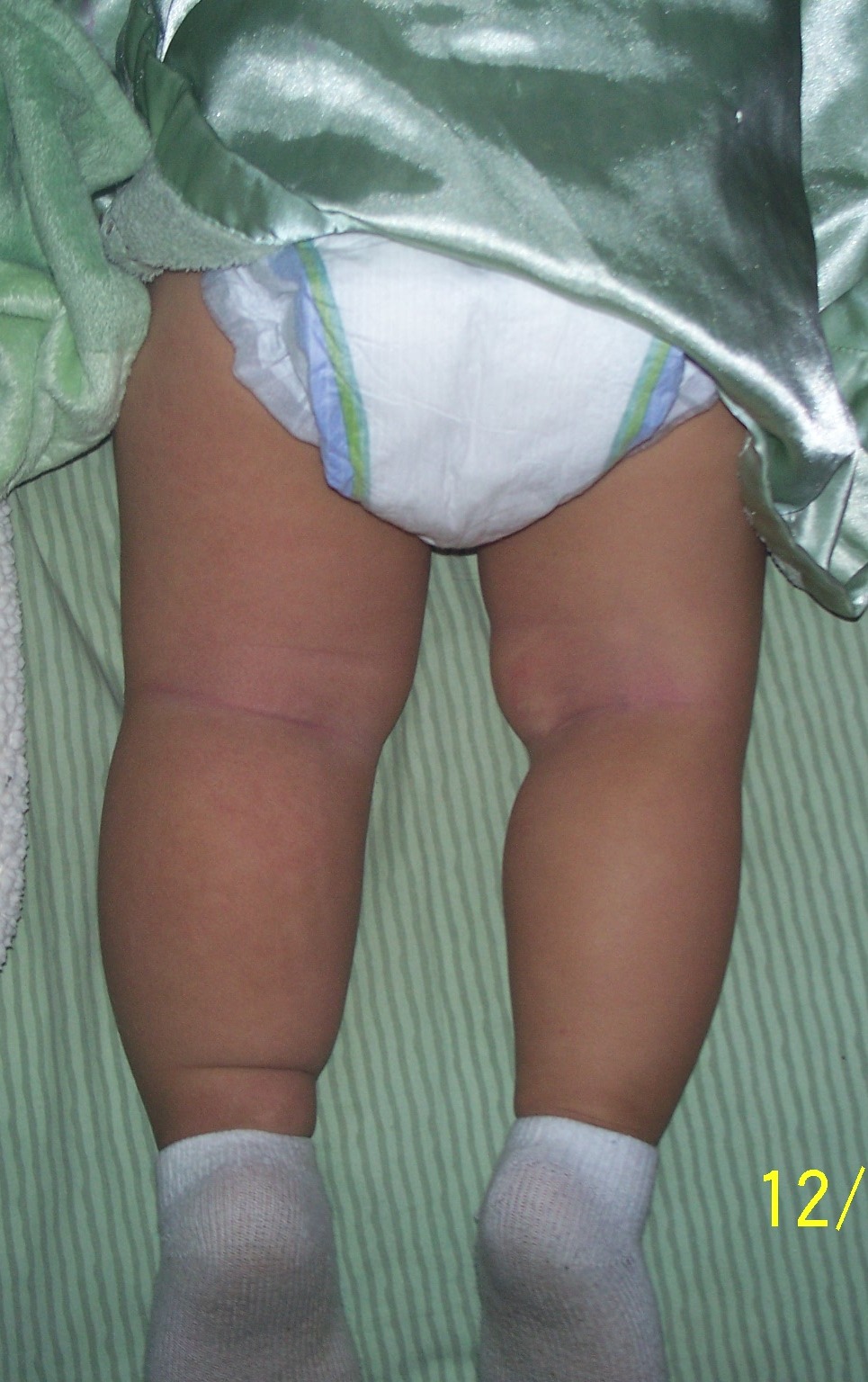
G. è
una bella bimba di 4 mesi. Giunge al nostro ambulatorio per una
visita di controllo e la mamma ci fa notare che la bimba ha una
gambina più grossa dellaltra (Figura
1). La piccola è nata a termine da gravidanza normodecorsa
e di peso adeguato alletà gestazionale (3,25 Kg); è
allattata al seno, cresce regolarmente e alleco anche,
effettuata per screening, è stato rilevato un ritardo della
maturazione coxofemorale a dx.
Durante
la visita di controllo i suoi dati antropometrici risultano nella
norma: peso 5,480 Kg (25°-50°), altezza 57,3 cm (10°),
circonferenza cranica 41cm (50-75°).
Allesame
obiettivo è evidente la lieve sproporzione tra gli arti
inferiori con asimmetria delle pliche cutanee confermata da
unaccurata misurazione (circonferenza coscia sinistra: 16,5 cm
vs destra: 16 cm; circonferenza gamba sinistra: 16,5 cm vs destra: 16
cm; piede sinistro: 11 cm vs destro: 10,5 cm). Oltre
allemi-iperplasia della gamba sinistra, la bimba non presenta
altri dati obiettivi patologici (dismorfismi, visceromegalia, lesioni
cutanee quali angiomi o nevi).
Lemi-iperplasia
può essere:
- congenita isolata (HHI iperplasia congenita isolata);
- parte di una sindrome da eccessiva crescita (SEC);
- secondaria a linfedema cronico, malformazioni linfangiomatose.
A questo
punto facciamo praticare alla piccola paziente delle indagini
strumentali:
- Eco addome e reni (per escludere la presenza di visceromegalia, nefrocalcinosi o malformazioni renali presenti nella S. di Beckwith-Wiedemann, SBW);
- Eco-color-doppler arti inferiori (per la possibilità che liperplasia fosse secondaria a linfedema).
Escluse
le cause secondarie di ipertrofia dellarto inviamo la bimba ad
effettuare una consulenza genetica. La motivazione è
dovuta al fatto che nellemi-iperplasia, sia isolata che
associata ad un quadro sindromico di eccessiva crescita, il rischio
tumorale è notevolmente aumentato, soprattutto nei primi
anni di vita. Per tale motivo la diagnosi aiuta nel programmare il
follow-up a cui deve essere sottoposta la piccola paziente. La
consulenza genetica esclude che la piccola sia affetta da una SEC.
La
bambina presenta un criterio maggiore (lemi-ipertrofia) per
porre diagnosi di SBW ma i dati anamnestici, obiettivi e strumentali
escludono la presenza di altri dati che permettano di avvalorare tale
ipotesi. Stesso discorso per le altre SEC quali: s. di
Klippel-Trenaunay-Weber, s. di Sotos, s. di Proteus etc.
Viene
dunque posta la diagnosi di Emi-iperplasia isolata semplice1.
Tale
patologia ha unincidenza di 1/86.000 nati, è
caratterizzata da asimmetria somatica, che può riguardare una
o più parti del corpo, solitamente visibile alla nascita e che
tende ad accentuarsi durante ladolescenza, e da un aumentato
rischio tumorale (5,9 volte più frequente rispetto ai non
affetti)2.
I tumori
più frequentemente associati a questa condizione,
perlopiù di origine embrionale, sono, in ordine di frequenza:
- Tumore di Wilms;
- Epatoblastoma;
- Carcinoma del surrene;
- Neuroblastoma;
- Feocromocitoma;
- Sarcomi indifferenziati.
Si è
trovato un consenso tra epidemiologi e genetisti: si sa che la fascia
detà a rischio sono i primi tre anni. Tuttavia,
è opportuno eseguire indagini più frequenti fino agli 8
anni e continuare con controlli distanziati fino alladolescenza.
Così fino a 8 anni è opportuno eseguire
periodicamente:
- un attento esame obiettivo semestrale (con particolare attenzione alladdome e ai dati antropometrici);
- un esame delle urine per riscontrare la presenza di marker (lacido vanilmandelico e lacido omovanilico per il neuroblastoma e lalfafetoproteina per lepatoblastoma) da effettuare ogni sei mesi;
- eco addome e rene (da praticare ogni tre mesi).
In
seguito i controlli possono essere diradati ma i pazienti vanno,
comunque, tenuti sotto osservazione clinica fino a sviluppo ultimato.
In particolare nel caso specifico della nostra piccola paziente, che
presenta emipertrofia a carico di un arto inferiore, durante la
crescita va valutata la sproporzione longitudinale degli arti che
tende ad accentuarsi con letà.
Questo
caso ci ha insegnato che:
- le malattie rare non sono poi così rare: le malattie genetiche sono rare se prese singolarmente ma, nel loro insieme, hanno un grosso impatto sulla casistica pediatrica. Inoltre con lavanzare della ricerca il loro numero è destinato ad aumentare nel tempo. Basti pensare che negli anni 60, quando nacque lOMIM (Online-Mendelian-Inheritance-in-Man) conteneva meno di 2000 entries, ma grazie ai notevoli progressi effettuati nella genetica medica tale numero è lievitato esponenzialmente fino alle 20.176 entità nosologiche attuali.
- Il ruolo di filtro diagnostico del pediatra di famiglia: dinnanzi a patologie rare o di recente classificazione nosologica il pediatra deve essere in grado formulare un corretto sospetto diagnostico, effettuare indagini diagnostiche di primo livello ed inviare il paziente al Centro di Riferimento.
Bibliografia
1. OMIM
235000 HEMIHYPERPLASIA, ISOLATED; IH. HEMI-3
SYNDROME, INCLUDED. Gene map locus 11p15.
2.
Hoyme HE, Seaver LH, Jones KL, Procopio F, Crooks W, Feingold M.
Isolated hemihyperplasia (hemihypertrophy): report of a prospective
multicenter study of the incidence of neoplasia and review. Am
J Med Genet 1998;79: 2748.
Vuoi citare questo contributo?